क्षारीय पृथ्वी धातुओं का उपयोग। क्षार धातु के यौगिक और उनके अनुप्रयोग। क्षारीय पृथ्वी धातु आयनों का उपयोग करके गुणात्मक प्रतिक्रियाएं

रासायनिक गुण क्षार और क्षारीय पृथ्वी धातु समान हैं। क्षार धातुओं के बाहरी ऊर्जा स्तर पर एक इलेक्ट्रॉन, क्षारीय पृथ्वी धातुएं हैं - दो। प्रतिक्रियाओं के दौरान, धातु आसानी से वैलेंस इलेक्ट्रॉनों के साथ भाग लेते हैं, एक मजबूत कम करने वाले एजेंट के गुणों को दिखाते हैं।
क्षारीय
आवर्त सारणी के समूह I में क्षार धातुएं शामिल हैं:
- लिथियम;
- सोडियम;
- पोटैशियम;
- rubidium;
- सीज़ियम;
- फ्रैनशियम।

चित्र: 1. क्षार धातु।
वे नरम होते हैं (चाकू से काटा जा सकता है), कम पिघलने और उबलते बिंदु। ये सबसे सक्रिय धातु हैं।
क्षार धातुओं के रासायनिक गुणों को तालिका में प्रस्तुत किया गया है।
|
प्रतिक्रिया |
विशेषताएं: |
समीकरण |
|
ऑक्सीजन के साथ |
हवा में जल्दी से ऑक्सीकरण करता है। लिथियम 200 डिग्री सेल्सियस से ऊपर के तापमान पर एक ऑक्साइड बनाता है। सोडियम 80% पेरोक्साइड (R 2 O 2) और 20% ऑक्साइड का मिश्रण बनाता है। बाकी धातुएं सुपरऑक्साइड (आरओ 2) बनाती हैं |
4Li + O 2 → 2Li 2 O; 2Na + O 2 → Na 2 O 2; आरबी + ओ २ → आरबीओ २ |
|
केवल कमरे के तापमान पर लिथियम को प्रतिक्रिया करता है |
6 एलआई + एन 2 → 2 एलआई 3 एन |
|
|
हलोजन के साथ |
प्रतिक्रिया हिंसक है |
2Na + Cl 2 → 2NaCl |
|
गैर-धातुओं के साथ |
जब गर्म किया जाता है। फार्म सल्फाइड, हाइड्राइड, फॉस्फाइड, सिलिकाइड। कार्बन के साथ केवल लिथियम और सोडियम प्रतिक्रिया करते हैं, कार्बाइड बनाते हैं |
2K + एस → के 2 एस; 2Na + H 2 → 2NaH; 2C + 5P → Cs 2 P 5; आरबी + सी → आरबीएसआई; 2 एलआई + 2 सी → ली 2 सी 2 |
|
केवल लिथियम शांति से प्रतिक्रिया करता है। पीली आंच से सोडियम जलता है। पोटेशियम एक फ्लैश के साथ प्रतिक्रिया करता है। सीज़ियम और रुबिडियम में विस्फोट होता है |
2Na + 2H 2 O → 2NaOH + H 2 - |
|
|
एसिड के साथ |
हाइड्रोक्लोरिक, फॉस्फोरिक, पतला सल्फ्यूरिक एसिड के साथ, वे विस्फोटक रूप से प्रतिक्रिया करते हैं। जब केंद्रित सल्फ्यूरिक एसिड के साथ प्रतिक्रिया होती है, तो हाइड्रोजन सल्फाइड रिलीज होता है, केंद्रित नाइट्रिक एसिड के साथ यह नाइट्रिक ऑक्साइड (I) बनाता है, पतला नाइट्रिक एसिड के साथ - नाइट्रोजन |
2Na + 2HCl → 2NaCl + H 2; 8Na + 5H 2 SO 4 (संक्षिप्त) → 4Na 2 SO 4 + H 2 S + 4H 2 O; 8K + 10HNO 3 (संक्षिप्त) → 8KNO 3 + N 2 O + 5H 2 O; 10Na + 12HNO 3 (पतला) → N 2 + 10NaNO 3 + 6H 2 O |
|
अमोनिया के साथ |
प्रपत्र अमीनों |
2 एलआई + 2 एनएच 3 → 2 एलआईएनएच 2 + एच 2 |
कार्बनिक अम्ल और अल्कोहल के साथ प्रतिक्रिया कर सकते हैं।
क्षारीय मृदा
क्षारीय पृथ्वी धातु आवर्त सारणी के समूह II में हैं:
- बेरिलियम;
- मैग्नीशियम;
- कैल्शियम;
- स्ट्रोंटियम;
- बेरियम;
- रेडियम।

चित्र: 2। क्षारीय पृथ्वी धातु.
क्षार धातुओं के विपरीत, वे कठिन हैं। केवल स्ट्रोंटियम को चाकू से काटा जा सकता है। सघन धातु रेडियम (5.5 ग्राम / सेमी 3) है।
बेरिलियम 900 ° C तक गर्म होने पर ही ऑक्सीजन के साथ क्रिया करता है। किसी भी परिस्थिति में हाइड्रोजन और पानी के साथ प्रतिक्रिया नहीं करता है। मैग्नीशियम 650 ° C पर ऑक्सीकरण करता है और उच्च दबाव पर हाइड्रोजन के साथ प्रतिक्रिया करता है।
तालिका क्षारीय पृथ्वी धातुओं के मुख्य रासायनिक गुणों को दर्शाती है।
|
प्रतिक्रिया |
विशेषताएं: |
समीकरण |
|
ऑक्सीजन के साथ |
फॉर्म ऑक्साइड फिल्में। 500 डिग्री सेल्सियस तक गर्म होने पर, अनायास प्रज्वलित करें |
2 एमजी + ओ 2 → 2 एमजीओ |
|
हाइड्रोजन के साथ |
उच्च तापमान पर फार्म हाइड्राइड्स |
Sr + H 2 → SrH 2 |
|
हैलोजन और गैर-धातुओं के साथ |
गर्म होने पर प्रतिक्रिया करें |
Be + Cl 2 → BeCl 2; Mg + S → MgS; 3Ca + 2P → Ca 3 P 2; 3a + एन 2 → सीए 3 एन 2; बा + २ सी → बासी २ |
|
कमरे के तापमान पर |
Mg + 2H 2 O → Mg (OH) 2 + H 2 |
|
|
एसिड के साथ |
सभी धातुएं लवण बनाने के लिए प्रतिक्रिया करती हैं |
4Ca + 10HNO 3 (संक्षिप्त) → 4Ca (NO 3) 2 + N 2 O + 5H 2 O |
|
क्षार के साथ |
केवल बेरिलियम प्रतिक्रिया करता है |
Be + 2NaOH + 2H 2 O → Na 2 + H 2 |
|
प्रतिस्थापन |
ऑक्साइड में कम सक्रिय धातुओं की जगह। एक अपवाद बेरिलियम है |
2Mg + ZrO 2 → Zr + 2MgO |
लवणों में क्षार और क्षारीय पृथ्वी धातुओं के आयनों को आसानी से लौ के रंग में परिवर्तन से पता लगाया जाता है। सोडियम लवण एक पीले रंग की लौ, पोटेशियम - वायलेट, रूबिडियम - लाल, कैल्शियम - ईंट लाल, बेरियम - पीले-हरे रंग के साथ जलता है। इन धातुओं के लवण का उपयोग आतिशबाजी बनाने के लिए किया जाता है।

चित्र: 3. गुणात्मक प्रतिक्रिया।
हमने क्या सीखा है?
क्षार और क्षारीय पृथ्वी धातु आवर्त सारणी के सक्रिय तत्व हैं जो सरल और के साथ प्रतिक्रिया करते हैं जटिल पदार्थ... क्षार धातुएं नरम होती हैं, पानी और हैलोजन के साथ हिंसक प्रतिक्रिया करती हैं, आसानी से हवा में ऑक्सीकरण करती हैं, ऑक्साइड, पेरोक्साइड, सुपरऑक्साइड का निर्माण करती हैं, एसिड और अमोनिया के साथ बातचीत करती हैं। गर्म होने पर, वे गैर-धातुओं के साथ प्रतिक्रिया करते हैं। क्षारीय पृथ्वी धातुएं गैर-धातुओं, एसिड, पानी के साथ प्रतिक्रिया करती हैं। बेरिलियम हाइड्रोजन और पानी के साथ बातचीत नहीं करता है, लेकिन उच्च तापमान पर क्षार और ऑक्सीजन के साथ प्रतिक्रिया करता है।
विषय द्वारा परीक्षण
रिपोर्ट का आकलन
औसत रेटिंग: 4.3। कुल रेटिंग प्राप्त हुई: 113
क्षारीय पृथ्वी धातु और, क्षारीय पृथ्वी धातु रसायनक्षारीय पृथ्वी धातु - तत्वों की आवर्त सारणी के दूसरे समूह के रासायनिक तत्व: कैल्शियम, स्ट्रोंटियम, बेरियम और रेडियम।
- 1 भौतिक गुण
- 2 रासायनिक गुण
- २.१ सरल पदार्थ
- २.२ आक्साइड
- 2.3 हाइड्रॉक्साइड्स
- 3 प्रकृति में होना
- 4 जैविक भूमिका
- 5 नोट्स
भौतिक गुण
क्षारीय पृथ्वी धातुओं में केवल कैल्शियम, स्ट्रोंटियम, बेरियम और रेडियम शामिल हैं, कम अक्सर मैग्नीशियम। इस उपसमूह का पहला तत्व बेरिलियम, इसके अधिकांश गुणों में, समूह के उच्च एनालॉग्स की तुलना में एल्यूमीनियम के बहुत करीब है, जो इसके अंतर्गत आता है। इस समूह में दूसरा तत्व, मैग्नीशियम, कुछ मामलों में क्षारीय पृथ्वी धातुओं से कई रासायनिक गुणों में काफी भिन्न होता है। सभी क्षारीय पृथ्वी धातु ग्रे, कमरे के तापमान के पदार्थों में ठोस हैं। क्षार धातुओं के विपरीत, वे बहुत कठिन होते हैं, और ज्यादातर चाकू से काटे नहीं जाते हैं (अपवाद स्ट्रोंटियम है। क्षारीय पृथ्वी धातुओं के घनत्व में वृद्धि केवल कैल्शियम के साथ शुरू होती है। सबसे भारी रेडियम है, जो कि जर्मेनियम (ρ \u003d 5.5 g / cm3) के घनत्व में तुलनीय है। ...
| परमाणु संख्या |
नाम, प्रतीक |
प्राकृतिक आइसोटोप | परमाणु भार | आयनीकरण ऊर्जा, केजे मोल - 1 | इलेक्ट्रॉन आत्मीयता, केजे मोल - 1 | ईओ | धातु। त्रिज्या, एनएम | आयनिक त्रिज्या, एनएम | tPL, ° C |
tboil, ° C |
ρ, जी / सेमी³ |
Δहप्ल, केजे मोल - १ | Boहोबिल, केजे मोल - १ |
|---|---|---|---|---|---|---|---|---|---|---|---|---|---|
| 4 | बेरिलियम होना | 1 + 11 ए | 9,012182 | 898,8 | 0,19 | 1,57 | 0,169 | 0,034 | 1278 | 2970 | 1,848 | 12,21 | 309 |
| 12 | मैग्नीशियम मिलीग्राम | 3 + 19 ए | 24,305 | 737,3 | 0,32 | 1,31 | 0,24513 | 0,066 | 650 | 1105 | 1,737 | 9,2 | 131,8 |
| 20 | कैल्शियम सी | 5 + 19 ए | 40,078 | 589,4 | 0,40 | 1,00 | 0,279 | 0,099 | 839 | 1484 | 1,55 | 9,20 | 153,6 |
| 38 | स्ट्रोंटियम सीनियर | 4 + 35 ए | 87,62 | 549,0 | 1,51 | 0,95 | 0,304 | 0,112 | 769 | 1384 | 2,54 | 9,2 | 144 |
| 56 | बेरियम बा | 7 + 43 ए | 137,327 | 502,5 | 13,95 | 0,89 | 0,251 | 0,134 | 729 | 1637 | 3,5 | 7,66 | 142 |
| 88 | रेडियम रा | 46a | 226,0254 | 509,3 | - | 0,9 | 0,2574 | 0,143 | 700 | 1737 | 5,5 | 8,5 | 113 |
एक रेडियोधर्मी आइसोटोप
रासायनिक गुण
क्षारीय पृथ्वी धातुओं में बाह्य ऊर्जा स्तर ns and का एक इलेक्ट्रॉनिक विन्यास होता है, और ये क्षार धातुओं के साथ-साथ तत्व भी होते हैं। दो वैलेंस इलेक्ट्रॉनों के होने पर, क्षारीय पृथ्वी धातुएं उन्हें आसानी से दूर कर देती हैं, और सभी यौगिकों में उनका ऑक्सीकरण राज्य +2 (बहुत कम ही +1) होता है।
क्षारीय पृथ्वी धातुओं की रासायनिक गतिविधि बढ़ती सीरियल संख्या के साथ बढ़ जाती है। कॉम्पैक्ट रूप में बेरिलियम या तो ऑक्सीजन या हैलोजन के साथ प्रतिक्रिया नहीं करता है, यहां तक \u200b\u200bकि लाल गर्मी के तापमान पर (600 डिग्री सेल्सियस तक, ऑक्सीजन और अन्य चाकोजेनेस के साथ प्रतिक्रिया के लिए, और भी अधिक तपिश, फ्लोरीन एक अपवाद है)। मैग्नीशियम कमरे के तापमान और अधिक (650 डिग्री सेल्सियस तक) के तापमान पर एक ऑक्साइड फिल्म द्वारा संरक्षित है और आगे ऑक्सीकरण नहीं करता है। कैल्शियम को धीरे-धीरे कमरे के तापमान पर (जल वाष्प की उपस्थिति में) अंदर की ओर ऑक्सीकरण किया जाता है, और ऑक्सीजन में थोड़ी सी गर्मी के साथ जलता है, लेकिन कमरे के तापमान पर शुष्क हवा में स्थिर होता है। स्ट्रोंटियम, बेरियम और रेडियम तेजी से हवा में ऑक्सीकृत होते हैं, ऑक्साइड और नाइट्राइड का मिश्रण देते हैं, इसलिए वे क्षार धातुओं और कैल्शियम की तरह, मिट्टी के तेल की एक परत के नीचे जमा होते हैं।
इसके अलावा, क्षार धातुओं के विपरीत, क्षारीय पृथ्वी धातु सुपरऑक्साइड और ओजोनाइड्स नहीं बनाते हैं।
क्षारीय पृथ्वी धातुओं के ऑक्साइड और हाइड्रॉक्साइड धारावाहिक संख्या बढ़ाने के साथ अपने मूल गुणों को बढ़ाते हैं।
साधारण पदार्थ
बेरिलियम कमजोर और के साथ प्रतिक्रिया करता है मजबूत समाधान लवण के निर्माण के साथ अम्ल:
हालांकि, ठंड केंद्रित नाइट्रिक एसिड के साथ पारित कर दिया।
क्षार के जलीय घोल के साथ बेरिलियम की प्रतिक्रिया हाइड्रोजन के विकास और हाइड्रॉक्सीबेरिलेट्स के निर्माण के साथ होती है:
400-500 ° C पर पिघले हुए क्षार के साथ अभिक्रिया करने पर, डाइऑक्सोबेरीयलेट बनते हैं:
मैग्नीशियम, कैल्शियम, स्ट्रोंटियम, बेरियम और रेडियम पानी के साथ क्षार बनाने के लिए प्रतिक्रिया करते हैं (मैग्नीशियम को छोड़कर, जो केवल पानी के साथ प्रतिक्रिया करता है जब एक गर्म मैग्नीशियम पाउडर पानी में जोड़ा जाता है):
इसके अलावा, कैल्शियम, स्ट्रोंटियम, बेरियम और रेडियम हाइड्रोजन, नाइट्रोजन, बोरान, कार्बन और अन्य गैर-धातुओं के साथ प्रतिक्रिया करते हैं ताकि संबंधित द्विआधारी यौगिक बन सकें:
आक्साइड
बेरिलियम ऑक्साइड एक एम्फ़ोटेरिक ऑक्साइड है जो लवण बनाने के लिए केंद्रित खनिज एसिड और क्षार में घुल जाता है:
लेकिन कम मजबूत एसिड और ठिकानों के साथ, प्रतिक्रिया अब आगे नहीं बढ़ती है।
मैग्नीशियम ऑक्साइड पतला और केंद्रित क्षारों के साथ प्रतिक्रिया नहीं करता है, लेकिन आसानी से एसिड और पानी के साथ प्रतिक्रिया करता है:
कैल्शियम, स्ट्रोंटियम, बेरियम और रेडियम के ऑक्साइड मूल ऑक्साइड हैं जो पानी, एसिड और एम्फ़ोटेरिक ऑक्साइड और हाइड्रॉक्साइड के मजबूत और कमजोर समाधानों के साथ प्रतिक्रिया करते हैं:
हाइड्रॉक्साइड
बेरिलियम हाइड्रॉक्साइड एम्फ़ोटेरिक है, जब मजबूत आधारों के साथ प्रतिक्रिया करते हुए बेरिलेट्स बनते हैं, एसिड के साथ - एसिड के बेरिलियम लवण:
मैग्नीशियम, कैल्शियम, स्ट्रोंटियम, बेरियम और रेडियम के हाइड्रॉक्साइड्स कुर्सियां \u200b\u200bहैं, ताकत कमजोर से बहुत मजबूत तक बढ़ जाती है, जो सबसे मजबूत संक्षारक पदार्थ है, जो गतिविधि में पोटेशियम हाइड्रॉक्साइड से अधिक है। वे पानी में अच्छी तरह से भंग कर देते हैं (मैग्नीशियम और कैल्शियम हाइड्रॉक्साइड को छोड़कर)। वे एसिड के साथ प्रतिक्रियाओं की विशेषता है और अम्लीय आक्साइड और एम्फ़ोटेरिक ऑक्साइड और हाइड्रॉक्साइड के साथ:
प्रकृति में होना
सभी क्षारीय पृथ्वी धातुएं (अलग-अलग मात्रा में) प्रकृति में पाई जाती हैं। उनकी उच्च रासायनिक गतिविधि के कारण, वे सभी एक स्वतंत्र अवस्था में नहीं होते हैं। सबसे आम क्षारीय पृथ्वी धातु कैल्शियम है, जिसकी मात्रा 3.38% (पृथ्वी की पपड़ी के द्रव्यमान का) है। मैग्नीशियम इससे थोड़ा कम है, जिसकी मात्रा 2.35% (पृथ्वी की पपड़ी के द्रव्यमान) है। बेरियम और स्ट्रोंटियम भी प्रकृति में व्यापक हैं, जिनमें से क्रमशः पृथ्वी की पपड़ी के द्रव्यमान का 0.05 और 0.034% है। बेरिलियम एक दुर्लभ तत्व है, जिसकी मात्रा पृथ्वी की पपड़ी के द्रव्यमान का 6 × 10 %4% है। रेडियम के लिए, जो रेडियोधर्मी है, यह सभी क्षारीय पृथ्वी धातुओं में सबसे दुर्लभ है, लेकिन यह हमेशा यूरेनियम अयस्कों में कम मात्रा में पाया जाता है। विशेष रूप से, इसे रासायनिक साधनों से वहां से अलग किया जा सकता है। इसकी सामग्री 1 · 10−10% (पृथ्वी की पपड़ी के द्रव्यमान) के बराबर है।
जैविक भूमिका
मैग्नीशियम जानवरों और पौधों (क्लोरोफिल) के ऊतकों में पाया जाता है, कई एंजाइमी प्रतिक्रियाओं का एक सहसंयोजक है, एटीपी के संश्लेषण में आवश्यक है, तंत्रिका आवेगों के संचरण में भाग लेता है, और सक्रिय रूप से दवा (बिस्कोफिटोथेरेपी, आदि) में उपयोग किया जाता है। कैल्शियम पौधों, जानवरों और मनुष्यों में एक सामान्य मैक्रोन्यूट्रिएंट है। मानव शरीर और अन्य कशेरुक, इसका अधिकांश हिस्सा कंकाल और दांतों में है। हड्डियों में हाइड्रॉक्सीपैटाइट के रूप में कैल्शियम होता है। का अलग - अलग रूप कैल्शियम कार्बोनेट (चूना) अकशेरुकी (स्पंज, प्रवाल पॉलीप्स, मोलस्क, आदि) के अधिकांश समूहों के "कंकाल" हैं। कैल्शियम आयन रक्त जमावट प्रक्रियाओं में शामिल होते हैं, और कोशिकाओं के भीतर सार्वभौमिक माध्यमिक दूतों में से एक के रूप में भी काम करते हैं और विभिन्न प्रकार के इंट्रासेल्युलर प्रक्रियाओं को विनियमित करते हैं - मांसपेशियों में संकुचन, एक्सोसाइटोसिस, जिसमें हार्मोन और न्यूरोट्रांसमीटर का स्राव शामिल है। स्ट्रोंटियम कैल्शियम को प्राकृतिक ऊतकों में बदल सकता है, क्योंकि यह गुणों में इसके समान है। मानव शरीर, स्ट्रोंटियम का द्रव्यमान कैल्शियम के द्रव्यमान का लगभग 1% है।
फिलहाल, बेरिलियम, बेरियम और रेडियम की जैविक भूमिका के बारे में कुछ भी ज्ञात नहीं है। बेरियम और बेरिलियम के सभी यौगिक जहरीले होते हैं। रेडियम अत्यंत रेडियोटॉक्सिक है। यह शरीर में कैल्शियम की तरह व्यवहार करता है - शरीर में प्रवेश करने वाले रेडियम का लगभग 80% हड्डी ऊतक में जमा होता है। रेडियम की उच्च सांद्रता ऑस्टियोपोरोसिस, सहज अस्थि भंग, और हड्डियों और घातक ऊतक के घातक ट्यूमर का कारण बनती है। रेडियम का एक गैसीय रेडियोधर्मी क्षय उत्पाद रेडॉन भी खतरनाक है।
टिप्पणियाँ
- नए IUPAC वर्गीकरण के अनुसार। पुरानी वर्गीकरण के अनुसार, वे आवर्त सारणी के समूह II के मुख्य उपसमूह से संबंधित हैं।
- अकार्बनिक रसायन विज्ञान का नामकरण। IUPAC अनुशंसाएँ 2005. - इंटरनेशनल यूनियन ऑफ़ प्योर एंड एप्लाइड केमिस्ट्री, 2005. - पी। 51।
- समूह 2 - क्षारीय पृथ्वी धातु, रसायन विज्ञान की रॉयल सोसायटी।
- गोल्ड फंड। स्कूल विश्वकोश। रसायन विज्ञान। एम।: बस्टर्ड, 2003।
| आवधिक प्रणाली रासायनिक तत्व डी। आई। मेंडेलीवा | ||||||||||||||||||||||||||||||||
|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|
| 1 | 2 | 3 | 4 | 5 | 6 | 7 | 8 | 9 | 10 | 11 | 12 | 13 | 14 | 15 | 16 | 17 | 18 | |||||||||||||||
| 1 | एच | वह | ||||||||||||||||||||||||||||||
| 2 | ली | होना | बी | सी | एन | हे | एफ | ne | ||||||||||||||||||||||||
| 3 | ना | मिलीग्राम | अल | सी | पी | एस | क्लोरीन | अर | ||||||||||||||||||||||||
| 4 | क | सीए | अनुसूचित जाति | ती | वी | सीआर | Mn | फे | सह | नी | Cu | Zn | गा | जीई | जैसा | Se | बीआर | Kr | ||||||||||||||
| 5 | Rb | सीनियर | Y | zr | नायब | मो | Tc | आरयू | आरएच | पी.डी. | एजी | सीडी | में | Sn | Sb | ते | मैं | XE | ||||||||||||||
| 6 | सी | बी 0 ए | ला | Ce | पीआर | एन डी | बजे | एस.एम. | यूरोपीय संघ | गोलों का अंतर | Tb | उप | हो | एर | Tm | Yb | लू | एचएफ | टा | डब्ल्यू | फिर से | ओएस | आईआर | पं | Au | एचजी | Tl | Pb | द्वि | पो | पर | आर एन |
| 7 | फादर | रा | एसी | गु | देहात | यू | Np | पु | Am | से। मी | बीके | सीएफ़ | Es | एफएम | मोहम्मद | नहीं। | एलआर | आरएफ | Db | Sg | Bh | एच | माउंट | डी एस | rg | Cn | Uut | Fl | UUP | Lv | नया | Uuo |
| 8 | UUE | UBN | Ubu | UBB | यूटीबी | Ubq | यूबीपी | Ubh | ||||||||||||||||||||||||
क्षारीय पृथ्वी धातु, क्षारीय पृथ्वी धातु और, क्षारीय पृथ्वी धातु रसायन, क्षारीय पृथ्वी धातु
भाग एक। सामान्य विशेषताएँ द्वितीयऔर तत्वों की आवर्त सारणी के समूह।
निम्नलिखित तत्व इस समूह में स्थित हैं: Be, Mg, Ca, Sr, Ba, Ra। उनके पास एक सामान्य इलेक्ट्रॉनिक कॉन्फ़िगरेशन है: (n-1) p 6 ns 2, Be 1s 2 2s 2 को छोड़कर। उत्तरार्द्ध के कारण, Be के गुण उपसमूह के गुणों से थोड़ा भिन्न होते हैं। मैग्नीशियम के गुण भी उपसमूह से भिन्न होते हैं, लेकिन कुछ हद तक। सीए - सीनियर - बा - राय श्रृंखला में, गुण क्रमिक रूप से बदलते हैं। Be - Ra श्रृंखला में सापेक्ष विद्युतीयता कम हो जाती है क्योंकि परमाणु आकार में वृद्धि के साथ, वैलेंस इलेक्ट्रॉनों को अधिक आसानी से दान किया जाता है। IIA उपसमूह तत्वों के गुणों को दो ns इलेक्ट्रॉनों को देने की आसानी से निर्धारित किया जाता है। इस स्थिति में, आयन E 2+ बनते हैं। एक्स-रे विवर्तन के अध्ययन में, यह पता चला कि कुछ यौगिकों में आईआईए उपसमूह के तत्व मोनोवलेंस प्रदर्शित करते हैं। ऐसे यौगिकों का एक उदाहरण ईजी है, जो ईजी 2 पिघल में ई जोड़कर प्राप्त किया जाता है। इस श्रृंखला के सभी तत्व अपनी उच्च गतिविधि के कारण मुक्त अवस्था में प्रकृति में नहीं पाए जाते हैं।
भाग दो। बेरिलियम और मैग्नीशियम।
बेरिलियम का इतिहास
प्राचीन पत्थरों के रूप में बेरिलियम यौगिकों को प्राचीन काल से जाना जाता है। लंबे समय से, लोगों ने नीले एक्वामरीन, हरे पन्ने, हरे-पीले बेरिल और गोल्डन क्राइसोबेरिल की जमा और खोज की है। लेकिन केवल 18 वीं शताब्दी के अंत में, केमिस्टों को संदेह था कि बेरिल में कुछ नया अज्ञात तत्व था। 1798 में, फ्रांसीसी रसायनज्ञ लुईस निकोलस वाओक्वेलिन ने बेरिल से ऑक्साइड "ला टेरी डु बेरिल" को अलग किया, जो एल्यूमिना से अलग था। इस ऑक्साइड ने लवणों को एक मीठा स्वाद प्रदान किया, फिटकिरी नहीं बनाई, अमोनियम कार्बोनेट के घोल में घुलने दिया और पोटेशियम ऑक्सालेट के साथ अवक्षेपण नहीं किया। मेटालिक बेरिलियम को पहली बार 1829 में प्रसिद्ध जर्मन वैज्ञानिक वेलर द्वारा प्राप्त किया गया था और उसी समय फ्रांसीसी वैज्ञानिक बसी, जिन्होंने धातु पोटेशियम के साथ बेरिलियम क्लोराइड को कम करके धातु बेरिलियम पाउडर प्राप्त किया था। औद्योगिक उत्पादन की शुरुआत 30-40 के दशक की है। पीछ्ली शताब्दी।
मैग्नीशियम इतिहास
तत्व को प्राचीन ग्रीस में मैग्नेशिया के क्षेत्र से अपना नाम मिला। निर्माण में लंबे समय से प्राकृतिक मैग्नीशियम युक्त सामग्री मैग्नेसाइट और डोलोमाइट का उपयोग किया गया है।
शुद्ध रूप में मैग्नेशिया के धातु आधार को अलग करने के पहले प्रयास 19 वीं शताब्दी की शुरुआत में किए गए थे। प्रसिद्ध अंग्रेजी भौतिक विज्ञानी और रसायनज्ञ हम्फ्री डेवी (1778-1829) के बाद उन्होंने पोटेशियम हाइड्रॉक्साइड और सोडियम हाइड्रॉक्साइड के इलेक्ट्रोलिस पिघल के अधीन किया और धात्विक Na और K प्राप्त किया। उन्होंने क्षारीय पृथ्वी धातुओं और मैग्नेशिया के ऑक्साइड के अपघटन को अंजाम देने के लिए इसी तरह से प्रयास करने का निर्णय लिया। अपने शुरुआती प्रयोगों में, डेवी ने गीले ऑक्साइड के माध्यम से एक करंट पास किया, जिससे उन्हें तेल की एक परत के साथ हवा के संपर्क में आने से रोका गया; हालाँकि, धातुओं को कैथोड के साथ जोड़ा गया था और उन्हें अलग नहीं किया जा सकता था।
डेवी ने कई अलग-अलग तरीकों की कोशिश की, लेकिन उनमें से सभी, विभिन्न कारणों से, असफल रहे। अंत में, 1808 में, वह भाग्यशाली था - उसने पारा ऑक्साइड के साथ गीला मैग्नेशिया मिलाया, एक प्लेटिनम प्लेट पर द्रव्यमान डाला और इसके माध्यम से एक करंट पारित किया; पारा निकालने के लिए गर्म किया गया, एक ग्लास ट्यूब में अमलगम को स्थानांतरित किया गया, और एक नई धातु प्राप्त की गई। उसी तरह, डेवी बेरियम, कैल्शियम और स्ट्रोंटियम प्राप्त करने में कामयाब रहे। जर्मनी में इलेक्ट्रोलाइटिक विधि से मैग्नीशियम का औद्योगिक उत्पादन 19 वीं शताब्दी के अंत में शुरू हुआ। हमारे देश में इलेक्ट्रोलाइटिक विधि द्वारा मैग्नीशियम के उत्पादन पर सैद्धांतिक और प्रायोगिक कार्य पी.पी. Fedot'ev; वैक्यूम में सिलिकॉन द्वारा मैग्नीशियम ऑक्साइड की कमी की प्रक्रिया का अध्ययन पी.एफ. Antipin।
फैलाव
बेरिलियम बहुत सामान्य तत्वों में से एक नहीं है: इसकी सामग्री पृथ्वी की ऊपरी तह 0.0004 wt है। %। प्रकृति में बेरिलियम एक बाध्य अवस्था में है। बेरिलियम के सबसे महत्वपूर्ण खनिज: बेरिल - 3 अल 2 (SiO 3) 6, क्राइसोबेरील - Be (AlO 2) 2 और फेनाकाइट - Be 2 SiO 4 हैं। अधिकांश बेरिलियम का छिड़काव कई अन्य तत्वों के खनिजों, विशेष रूप से एल्यूमीनियम के अशुद्धता के रूप में किया जाता है। बेरिलियम समुद्र के गहरे तलछट और कुछ कोयले की राख में भी पाया जाता है। बेरिल की कुछ किस्में, विभिन्न रंगों में अशुद्धियों के साथ रंग की, कीमती पत्थरों के रूप में वर्गीकृत की जाती हैं। ये हैं, उदाहरण के लिए, हरा पन्ना, हरी हरी एक्वामरीन।
मैग्नीशियम पृथ्वी की पपड़ी में सबसे प्रचुर तत्वों में से एक है। मैग्नीशियम सामग्री 1.4% है। सबसे महत्वपूर्ण खनिजों में, विशेष रूप से, कार्बोनिक कार्बोनेट चट्टानें हैं, जो भूमि और यहां तक \u200b\u200bकि पूरे पर्वत श्रृंखला पर विशाल द्रव्यमान बनाती हैं - मैग्नेसाइटMgCO 3 और डोलोमाइटMgCO 3 -CaCO 3। एक और आसानी से घुलनशील मैग्नीशियम युक्त खनिज के विशाल जमाव को विभिन्न जलोढ़ चट्टानों की परतों के नीचे जाना जाता है, साथ में पत्थर के जमाव के साथ - carnalliteMgCl 2 -KCl-6H 2 O. इसके अलावा, कई खनिजों में, मैग्नीशियम सिलिका के साथ घनिष्ठ रूप से जुड़ा हुआ है, उदाहरण के लिए, ओलीवाइन [(Mg, Fe) 2 SiO 4] और कम आम forsterite (Mg 2 SiO 4)। अन्य मैग्नीशियम युक्त खनिज हैं bruciteMg (OH) 2 , KieseriteMgSO 4 , epsoniteMgSO 4 -7H 2 हे , केनाइMgSO 4 -KCl-3H 2 हे . पृथ्वी की सतह पर, मैग्नीशियम आसानी से हाइड्रस सिलिकेट (तालक, एस्बेस्टोस, आदि) बनाता है, जिसका एक उदाहरण है टेढ़ा 3MgO-2SiO 2 -2H 2 O ज्ञात खनिजों का, लगभग 13% में मैग्नीशियम होता है। हालांकि, प्राकृतिक मैग्नीशियम यौगिक व्यापक रूप से भंग रूप में पाए जाते हैं। विभिन्न खनिजों और चट्टानों के अलावा, MgCl 2 के रूप में 0.13% मैग्नीशियम लगातार समुद्र के पानी में निहित है (इसका भंडार यहां अथाह है - लगभग 6-10 16 टन) और नमक झीलों और स्प्रिंग्स में। मैग्नीशियम भी 2% तक की मात्रा में क्लोरोफिल का एक हिस्सा है और यहां एक जटिल एजेंट के रूप में कार्य करता है। पृथ्वी के जीवित पदार्थ में इस तत्व की कुल सामग्री लगभग 10 11 टन अनुमानित है।
प्राप्त करना
मैग्नीशियम उत्पादन की मुख्य (लगभग 70%) विधि ऑक्सीकरण से बचाने के लिए फ्लक्स की एक परत के तहत पिघला हुआ कार्नालाइट या एमजीसीएल 2 की इलेक्ट्रोलिसिस है। मैग्नीशियम प्राप्त करने के लिए थर्मल विधि (लगभग 30%) निकाल मैग्नेसाइट या डोलोमाइट की कमी है। बेरिलियम सांद्रता बेरिलियम ऑक्साइड या हाइड्रोक्साइड में संसाधित किया जाता है, जिसमें से फ्लोराइड या क्लोराइड प्राप्त होता है। धात्विक बेरिलियम प्राप्त करते समय, BeCl 2 (50 wt।%) के एक पिघल के इलेक्ट्रोलिसिस और NaCl को बाहर किया जाता है। इस मिश्रण में शुद्ध BeCl 2 के लिए 300 ° C बनाम 400 ° C का गलनांक होता है। इसके अलावा, बेरिलियम को मैग्नीशियम - या एल्यूमोथर्मिक रूप से 1000-1200 0 C पर Na 2: Na 2 + 2Mg \u003d Be + 2Na + MgF 2 से प्राप्त किया जाता है। अत्यधिक शुद्ध बेरिलियम (मुख्य रूप से परमाणु उद्योग के लिए) ज़ोन पिघलने, वैक्यूम आसवन और इलेक्ट्रोलाइटिक शोधन द्वारा निर्मित होता है।
विशेषताएं:
बेरिलियम एक "शुद्ध" तत्व है। मैग्नीशियम स्वाभाविक रूप से तीन स्थिर समस्थानिकों के रूप में होता है: 24 Mg (78.60%), 25 Mg (10.11%) और 26 Mg (11.29%)। 23, 27 और 28 की संख्या वाले आइसोटोप कृत्रिम रूप से प्राप्त किए गए थे।
बेरिलियम का परमाणु क्रमांक 4 और परमाणु भार 9.0122 है। वह आवधिक प्रणाली की दूसरी अवधि में है और समूह 2 के मुख्य उपसमूह का प्रमुख है। बेरिलियम परमाणु की इलेक्ट्रॉनिक संरचना 1s 2 2s 2 है। रासायनिक बातचीत के दौरान बेरिलियम परमाणु उत्तेजित होता है (जिसमें 63 kcal / g × परमाणु की लागत की आवश्यकता होती है) और 2s-इलेक्ट्रॉनों में से एक को 2p-कक्षीय में स्थानांतरित किया जाता है, जो बेरिलियम के रसायन विज्ञान की विशिष्टता को निर्धारित करता है: यह विनिमय तंत्र द्वारा 2 बॉन्ड बनाते हुए 4 के अधिकतम सहसंयोजन का प्रदर्शन कर सकता है। और दाता-स्वीकर्ता के लिए 2। बेरिलियम आयनीकरण क्षमता वक्र पर ऊपरी पदों में से एक पर कब्जा कर लेता है। उत्तरार्द्ध अपनी छोटी त्रिज्या से मेल खाता है और बेरिलियम को एक तत्व के रूप में दर्शाता है जो विशेष रूप से अपने इलेक्ट्रॉनों को दान करने के लिए तैयार नहीं है, जो प्राथमिक रूप से तत्व की रासायनिक गतिविधि की कम डिग्री निर्धारित करता है। इलेक्ट्रोनगेटिविटी के दृष्टिकोण से, बेरिलियम को इलेक्ट्रोपोसिटिव धातु परमाणुओं के बीच एक विशिष्ट संक्रमण तत्व माना जा सकता है, जो आसानी से अपने इलेक्ट्रॉनों और विशिष्ट जटिल-गठन एजेंटों को दान करते हैं, जो बनने की प्रवृत्ति रखते हैं सहसंयोजक बंधन... बेरिलियम एल्युमिनियम के साथ एक विकर्ण सादृश्य दर्शाती है जो कि लाइसेंसएम से अधिक है और एक कैनोस्मिमेट्रिक तत्व है। बेरिलियम और इसके यौगिक अत्यधिक विषैले होते हैं। एमपीसी हवा में - 2 μg / m 3।
तत्वों की आवर्त सारणी में, मैग्नीशियम समूह II के मुख्य उपसमूह में स्थित है; मैग्नीशियम की क्रमिक संख्या 12 है, परमाणु भार 24.312। एक अस्पष्टीकृत परमाणु का इलेक्ट्रॉनिक विन्यास 1s 2 2s 2 2p 6 3s 2 है; बाहरी की संरचना इलेक्ट्रॉनिक गोले परमाणु Mg (3s 2) इसकी शून्य-वैधता अवस्था से मेल खाता है। द्विसंयोजक 3s 1 3p 1 के लिए उत्तेजना के लिए 62 kcal / g-atom की लागत की आवश्यकता होती है। मैग्नीशियम की आयनीकरण क्षमता बेरिलियम की तुलना में कम होती है, इसलिए, मैग्नीशियम यौगिकों की विशेषता होती है जो बंधन आक्सीकारक के उच्च अनुपात में होते हैं। जटिल क्षमता के संदर्भ में, मैग्नीशियम भी बेरिलियम से नीच है। अधूरा डी-शेल के साथ समूह IIIB तत्वों के साथ बातचीत में कुछ ख़ासियतें हैं। इस समूह में Sc, Y, Ln और Th शामिल हैं। ये तत्व मैग्नीशियम के साथ कई मध्यवर्ती चरण बनाते हैं और तरल अवस्था में इसमें अच्छे से घुल जाते हैं। मैग्नीशियम के साथ इन तत्वों के मिश्रण के राज्य आरेख eutectic प्रकृति के हैं। ठोस अवस्था में मैग्नीशियम में इन तत्वों की घुलनशीलता महान नहीं है (वजन से 2 - 5%)। क्षारीय पृथ्वी के साथ और विशेष रूप से क्षार धातुओं के साथ, मैग्नीशियम ठोस अवस्था में विलेयता का एक महत्वपूर्ण क्षेत्र नहीं बनाता है, जो परमाणु रेडी में एक बड़े अंतर से जुड़ा हुआ है। अपवाद लिथियम है, परमाणु त्रिज्या जिसमें मैग्नीशियम के परमाणु त्रिज्या 2% से भिन्न होता है। कॉपर, सिल्वर और गोल्ड के साथ मैग्नीशियम के सिस्टम यूटीक प्रकार के होते हैं। वजन के हिसाब से यूटीक तापमान -16% पर चांदी घुलनशीलता।
भौतिक गुण
फीरोज़ा - चांदी-सफेद धातु। काफी कठोर और नाजुक। इसमें डायनामैग्नेटिक गुण होते हैं। हवा में, यह एक पतली ऑक्साइड फिल्म के साथ कवर हो जाता है जो धातु को एक ग्रे, मैट रंग देता है और इसे आगे जंग से बचाता है। बेरिलियम की संपीडनशीलता बहुत कम है। सभी धातुओं का कम से कम (अल से 17 गुना कम) एक्स-रे विकिरण में देरी करता है। यह एचसीपी संरचना में पीरियड के साथ क्रिस्टलीकृत होता है, जिसमें अवधि \u003d 0.228 एनएम, और सी \u003d 0.358 एनएम, सीएन \u003d 6 होता है। 1254 डिग्री सेल्सियस पर, हेक्सागोनल का संशोधन एक घन बी में बदल जाता है। बेरिलियम अल और सी के साथ यूक्टेक्टिक मिश्र बनाता है।
प्रकृति में स्थिति
पृथ्वी की पपड़ी में बेरिलियम - 0.00053%, मैग्नीशियम - 1.95%, कैल्शियम - 3.38%, स्ट्रोंटियम - 0.014%, बेरियम - 0.026%, रेडियम - एक कृत्रिम तत्व है।
प्रकृति में केवल यौगिकों के रूप में पाया जाता है - सिलिकेट्स, एल्यूमिनोसिलिकेट्स, कार्बोनेट्स, फॉस्फेट्स, सल्फेट्स, आदि।
प्राप्त करने के
1. बेरिलियम फ्लोराइड की कमी से प्राप्त होता है:
BeF 2 + Mg t → C → Be + MgF 2
2. बेरियम ऑक्साइड की कमी से प्राप्त होता है:
3BO + 2Al t a C → 3Ba + Al 2 O 3
3. बाकी धातुएँ क्लोराइड पिघल के इलेक्ट्रोलिसिस द्वारा प्राप्त की जाती हैं:
चूंकि चूंकि इस उपसमूह की धातुएं मजबूत कम करने वाले एजेंट हैं, इसलिए उन्हें केवल पिघला हुआ नमक के इलेक्ट्रोलिसिस द्वारा प्राप्त करना संभव है। सीए के मामले में, सीएसीएल 2 का उपयोग आमतौर पर किया जाता है (पिघलने बिंदु को कम करने के लिए सीएएफ 2 के अतिरिक्त के साथ)
CaCl 2 \u003d Ca + Cl 2
भौतिक गुण
क्षारीय पृथ्वी धातुओं (क्षार धातुओं की तुलना में) में उच्च टी ° pl है। और टी ° गांठें, घनत्व और कठोरता।
आवेदन
| बेरिलियम (एम्फोटेरिन) | मैगनीशियम | सीए, सीनियर, बा, रा |
| 1. अंतरिक्ष के लिए गर्मी-परिरक्षण संरचनाओं का विनिर्माण। जहाजों (गर्मी प्रतिरोध, बेरिलियम की गर्मी क्षमता) 2. बेरिलियम कांस्य (हल्कापन, कठोरता, गर्मी प्रतिरोध, मिश्र धातुओं के विरोधी जंग, स्टील की तुलना में तन्य शक्ति, स्ट्रिप्स 0.1 मिमी मोटी में लुढ़का जा सकता है) 3. परमाणु रिएक्टरों में, एक्स-रे इंजीनियरिंग, रेडियो इलेक्ट्रॉनिक्स 4. मिश्र धातु , नी, डब्ल्यू- स्विस घड़ी स्प्रिंग्स बनाते हैं, लेकिन नाजुक, जहरीला और बहुत महंगा है | 1. धातु प्राप्त करना - मैग्नीशियम-थर्मल (टाइटेनियम, यूरेनियम, ज़िरकोनियम, आदि) 2. अल्ट्रा-लाइट मिश्र (विमान, ऑटोमोबाइल उत्पादन) प्राप्त करने के लिए 3. कार्बनिक संश्लेषण में 4. प्रकाश और आग लगाने वाले रॉकेट के निर्माण के लिए। | 1. बीयरिंगों के उत्पादन के लिए आवश्यक सीसा-कैडमियम मिश्र धातुओं का विनिर्माण। 2. स्ट्रोंटियम यूरेनियम उत्पादन में एक कम करने वाला एजेंट है। फॉस्फोरस स्ट्रोंटियम साल्ट हैं। 3. विद्युत उपकरणों में वैक्यूम बनाने के लिए गेटर्स, पदार्थों के रूप में उपयोग किया जाता है। कैल्शियम दुर्लभ धातुओं को प्राप्त करना, मिश्र धातुओं का एक हिस्सा है। कैथोड रे ट्यूब में बेरियम गेट्टर। रेडियम एक्स-रे निदान, अनुसंधान कार्य। |
रासायनिक गुण
1. बहुत प्रतिक्रियाशील, मजबूत कम करने वाले एजेंट। धातुओं की गतिविधि और उनकी कम करने की क्षमता निम्नलिखित क्रम में बढ़ जाती है: Be - Mg - Ca - Sr - Ba
2. +2 के एक ऑक्सीकरण स्थिति को रोकें।
3. हाइड्रोजन छोड़ने के लिए कमरे के तापमान (बी को छोड़कर) पर पानी के साथ प्रतिक्रिया करें।
4. हाइड्रोजन के साथ नमक जैसा हाइड्राइड ईएच 2।
5. ऑक्साइड में सामान्य सूत्र EO होता है। क्षार धातुओं की तुलना में पेरोक्साइड के निर्माण की प्रवृत्ति कम होती है।
पानी के साथ प्रतिक्रिया।
सामान्य परिस्थितियों में, Be और Mg की सतह एक अक्रिय ऑक्साइड फिल्म के साथ कवर होती है, इसलिए वे पानी के लिए प्रतिरोधी होती हैं, लेकिन साथ गर्म पानी मैग्नीशियम बेस Mg (OH) 2 बनाता है।
इसके विपरीत, Ca, Sr और Ba हाइड्रॉक्साइड बनाने के लिए पानी में घुलते हैं, जो मजबूत आधार हैं:
Be + H 2 O → बीओ + एच 2
सीए + 2 एच 2 ओ → सीए (ओएच) २ + एच २
ऑक्सीजन के साथ प्रतिक्रिया।
सभी धातुएँ आरओ ऑक्साइड, बेरियम रूप पेरोक्साइड - बाओ 2 बनाती हैं:
2 एमजी + ओ 2 → 2 एमजीओ
बा + ओ २ → बाओ २
3.बिना यौगिक अन्य गैर धातुओं के साथ बनता है:
Be + Cl 2 → BeCl 2 (पड़ाव)
बा + एस → बाएस (सल्फाइड)
3Mg + N 2 → Mg 3 N 2 (नाइट्राइड्स)
सीए + एच २ → सीएएच २ (हाइड्राइड्स)
सीए + 2 सी → सीएसी 2 (कार्बाइड)
3Ba + 2P → Ba 3 P 2 (फॉस्फाइड)
बेरिलियम और मैग्नीशियम गैर-धातुओं के साथ अपेक्षाकृत धीरे-धीरे प्रतिक्रिया करते हैं।
4. सभी धातुएं एसिड में घुल जाती हैं:
Ca + 2HCl → CaCl 2 + H 2
Mg + H 2 SO 4 (dil।) → MgSO 4 + H 2
बेरिलियम में भी घुल जाता है जलीय समाधान क्षार:
Be + 2NaOH + 2H 2 O → Na 2 + H 2
5. क्षारीय पृथ्वी धातुओं के उद्धरणों के लिए गुणात्मक प्रतिक्रिया - निम्नलिखित रंगों में लौ का रंग:
सीए 2+ - गहरा नारंगी
सीन 2+ - गहरा लाल
बा 2+ - हल्का हरा
बा 2+ कटियन आमतौर पर सल्फ्यूरिक एसिड या इसके लवण के साथ विनिमय प्रतिक्रिया द्वारा खोला जाता है:
BaCl 2 + H 2 SO 4 → BaSO 4 2 + 2HCl
Ba 2+ + SO 4 2- → BaSO 4 4
बेरियम सल्फेट एक सफेद अवक्षेप है, जो खनिज एसिड में अघुलनशील है।
क्षारीय पृथ्वी धातु आक्साइड
प्राप्त करना
1) धातुओं का ऑक्सीकरण (बा को छोड़कर, जो पेरोक्साइड बनाता है)
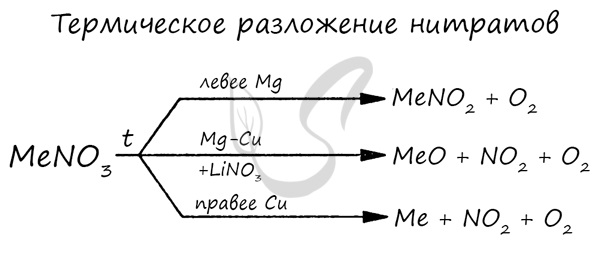
2) नाइट्रेट या कार्बोनेट का थर्मल अपघटन
सीएसीओ 3 टी → सी → सीएओ + सीओ 2
2Mg (NO 3) 2 t˚C → 2MgO + 4NO 2 + O 2
रासायनिक गुण
विशिष्ट बुनियादी ऑक्साइड। पानी (बीईओ और एमजीओ को छोड़कर), एसिड ऑक्साइड और एसिड के साथ प्रतिक्रिया करें
काओ + एच 2 ओ → सीए (ओएच) 2
3 सीएओ + पी 2 ओ 5 → सीए 3 (पीओ 4) 2
Beo + 2HNO 3 → Be (NO 3) 2 + H 2 O
बीईओ - एम्फोटेरिक ऑक्साइड, क्षार में घुलनशील:
बीईओ + 2 नोहा + एच 2 ओ → ना 2
क्षारीय पृथ्वी धातु हाइड्रॉक्साइड्स R (OH) 2
प्राप्त करना
क्षारीय पृथ्वी धातुओं या पानी के साथ उनके आक्साइड की प्रतिक्रियाएं:
बा + २ एच २ ओ → बा (ओएच) २ + एच २
CaO (क्विकटाइम) + H 2 O → Ca (OH) 2 (स्लेक्ड लाइम)
रासायनिक गुण
आर (ओएच) 2 हाइड्रॉक्साइड सफेद क्रिस्टलीय पदार्थ होते हैं, क्षार धातु हाइड्रॉक्साइड की तुलना में पानी में कम घुलनशील होते हैं ( घटते सीरियल नंबर के साथ हाइड्रोक्साइड्स की घुलनशीलता कम हो जाती है; Be (OH) 2 - पानी में अघुलनशील, क्षार में घुलनशील)। R (OH) 2 की मूलभूतता बढ़ती परमाणु संख्या के साथ बढ़ती है:
Be (OH) 2 - एम्फ़ोटेरिक हाइड्रॉक्साइड
Mg (OH) 2 - कमजोर आधार
सीए (ओएच) 2 - क्षार
बाकी हाइड्रॉक्साइड्स मजबूत आधार (क्षार) हैं।
1) अम्लीय ऑक्साइड के साथ प्रतिक्रिया:
Ca (OH) 2 + CO 2 → CaCO 3 H + H 2 O! कार्बन डाइऑक्साइड की गुणात्मक प्रतिक्रिया
बा (OH) 2 + SO 2 → BaSO 3 H + H 2 O
2) एसिड के साथ प्रतिक्रियाएं:
बा (OH) 2 + 2HNO 3 → बा (NO 3) 2 + 2H 2 O
3) लवण के साथ विनिमय की प्रतिक्रिया:
बा (OH) 2 + K 2 SO 4 → BaSO 4 2 + 2KOH
4) क्षारीय के साथ बेरिलियम हाइड्रॉक्साइड की प्रतिक्रिया:
Be (OH) 2 + 2NaOH → ना 2
पानी की कठोरता
Ca 2+ और Mg 2+ आयन वाले प्राकृतिक पानी को कठोर कहा जाता है। जब उबला हुआ, कठोर पानी बनता है, तो खाद्य उत्पाद इसमें नहीं उबलते हैं; डिटर्जेंट फोम नहीं करते हैं।
कार्बोनेट (अस्थायी) कठोरता पानी में कैल्शियम और मैग्नीशियम बाइकार्बोनेट की उपस्थिति के कारण, गैर-कार्बोनेट (निरंतर) कठोरता - क्लोराइड और सल्फेट।
कुल पानी की कठोरता कार्बोनेट और गैर-कार्बोनेट के योग के रूप में माना जाता है।
कठोरता को दूर करना पानी एक समाधान से सीए 2+ और एमजी 2+ आयनों की वर्षा द्वारा किया जाता है
क्षारीय पृथ्वी धातुओं में समूह IIa धातुएँ शामिल हैं: बेरिलियम, मैग्नीशियम, कैल्शियम, स्ट्रोंटियम, बेरियम और रेडियम। वे हल्केपन, कोमलता और मजबूत प्रतिक्रिया द्वारा विशेषता हैं।
सामान्य विशेषताएँ
बी से रा (ऊपर से नीचे तक) में आवर्त सारणी) वृद्धि हुई है: परमाणु त्रिज्या, धातु, बुनियादी, गुणों को कम करने, प्रतिक्रिया। इलेक्ट्रोनेटिविटी, आयनीकरण ऊर्जा, इलेक्ट्रॉन आत्मीयता को घटाता है।
इन तत्वों के इलेक्ट्रॉनिक विन्यास समान हैं, क्योंकि वे एक ही समूह में हैं (मुख्य उपसमूह!), सामान्य सूत्र 2 n है:
- हो - २ स २
- मिलीग्राम - 3 एस 2
- सीए - 4 एस 2
- सीनियर - 5 एस 2
- बा - ६ स २
- रा - 2 स २
प्राकृतिक यौगिक
प्रकृति में, क्षारीय पृथ्वी धातु निम्नलिखित यौगिकों में पाई जाती है:
- Be - BeO * Al 2 O 3 * 6SiO 2 - बेरिल
- Mg - MgCO 3 - मैग्नेसाइट, MgO * Al 2 O 3 - स्पिनेल, 2MgO * SiO 2 - ओलिविन
- सीए - सीएसीओ ३ - चाक, संगमरमर, चूना पत्थर, कैल्साइट, सीएएसओ ४ * २ एच २ ओ - जिप्सम, सीएएफ २ - फ्लोराइट

प्राप्त करना
ये सक्रिय धातुएँ हैं जिन्हें किसी समाधान के इलेक्ट्रोलिसिस द्वारा प्राप्त नहीं किया जा सकता है। उन्हें प्राप्त करने के लिए, पिघलने के इलेक्ट्रोलिसिस, एल्यूमिनोथर्मी और लवण से उनके विस्थापन को अन्य अधिक सक्रिय धातुओं द्वारा उपयोग किया जाता है।
MgCl 2 → (t) Mg + Cl 2 (पिघल इलेक्ट्रोलिसिस)
काओ + अल → अल 2 ओ 3 + सीए (एलुमिनाथमी एल्यूमीनियम के साथ अपने आक्साइड को कम करके धातुओं के उत्पादन की एक विधि है)
MgBr 2 + Ca → CaBr 2 + Mg

रासायनिक गुण

क्षारीय पृथ्वी धातु आक्साइड
उनके पास सामान्य सूत्र आरओ है, उदाहरण के लिए: एमजीओ, सीएओ, बीएओ।
प्राप्त करना
क्षारीय पृथ्वी धातु आक्साइड कार्बोनेट और नाइट्रेट के अपघटन द्वारा प्राप्त किया जा सकता है:
MgCO 3 → (t) MgO + CO 2
Ca (NO 3) 2 → (t) CaO + O 2 + NO 2
रासायनिक गुण
मुख्य रूप से मूल गुण दिखाएं, बीईओ को छोड़कर - एम्फ़ोटेरिक ऑक्साइड।

क्षारीय पृथ्वी धातु हाइड्रॉक्साइड
वे बेरिलियम हाइड्रॉक्साइड, एक एम्फ़ोटेरिक हाइड्रॉक्साइड के अपवाद के साथ बुनियादी गुण दिखाते हैं।
प्राप्त करना
हाइड्रॉक्साइड्स इसी धातु ऑक्साइड और पानी की प्रतिक्रिया में प्राप्त होते हैं (सभी को छोड़कर (ओएच) 2)
काओ + एच 2 ओ → सीए (ओएच) 2
रासायनिक गुण
अधिकांश हाइड्रॉक्साइड के मूल गुण एसिड और अम्लीय ऑक्साइड के साथ प्रतिक्रिया के लिए अनुकूल हैं।
बा (OH) 2 + H 2 SO 4 → BaSO 4 H + H 2 O
सीए (ओएच) 2 + एच 2 ओ + सीओ 2 → सीए (एचसीओ 3) 2 + एच 2 ओ
Ca (HCO 3) 2 + Ca (OH) 2 → CaCO 3 + H 2 O + CO 2
Ca (OH) 2 + CO 2 → CaCO 3 H + H 2 O

लवण के साथ प्रतिक्रिया (और न केवल) तब होती है जब नमक घुलनशील होता है और प्रतिक्रिया गैस के परिणामस्वरूप, एक अवक्षेप बनता है, या एक कमजोर इलेक्ट्रोलाइट (पानी) बनता है।
बा (OH) 2 + Na 2 SO 4 → BaSO 4 Na + NaOH
बेरिलियम हाइड्रॉक्साइड एम्फ़ोटेरिक है: यह दोहरे गुणों को प्रदर्शित करता है, एसिड और बेस दोनों के साथ प्रतिक्रिया करता है।
Be (OH) 2 + HCl → BeCl 2 + H 2 O
Be (OH) 2 + NaOH → Na 2
पानी की कठोरता पानी के गुणों का एक संयोजन है, इसमें मुख्य रूप से कैल्शियम और मैग्नीशियम लवण की उपस्थिति पर निर्भर करता है: हाइड्रोकार्बन, सल्फेट्स और क्लोराइड।
अस्थायी (कार्बोनेट) और स्थायी (गैर-कार्बोनेट) कठोरता के बीच भेद।

आप शायद घर पर पानी की कठोरता से निपटते हैं, मैं हर दिन हिम्मत करता हूं। केतली में पानी की साधारण उबलने से अस्थायी पानी की कठोरता समाप्त हो जाती है, और इसकी दीवारों पर चूना - CaCO 3 - कठोरता के उन्मूलन का निर्विवाद प्रमाण है:
Ca (HCO 3) 2 → CaCO 3 CO + CO 2 + H 2 O
इसके अलावा, पानी में Na 2 CO 3 जोड़कर अस्थायी कठोरता को समाप्त किया जा सकता है:
Ca (HCO 3) 2 + Na 2 CO 3 → CaCO 3 Na + NaHCO 3
उबलते हुए लगातार कठोरता से लड़ना बेकार है: उबालने के दौरान सल्फेट्स और क्लोराइड्स का वेग नहीं होगा। पानी में Na 2 CO 3 डालने से निरंतर पानी की कठोरता समाप्त हो जाती है:
CaCl 2 + Na 2 CO 3 → CaCO 3 Na + NaCl
MgSO 4 + Na 2 CO 3 + H 2 O → 2 CO 3 2 + CO 2 + Na 2 SO 4
विभिन्न परीक्षणों का उपयोग करके पानी की कठोरता का निर्धारण किया जा सकता है। अत्यधिक उच्च पानी की कठोरता बॉयलर, पाइप, केतली की दीवारों पर पैमाने के तेजी से गठन की ओर ले जाती है।

© बेल्वेलिच यूरी सर्गेइविच
यह लेख यूरी सर्गेइविच बेल्लेविच द्वारा लिखा गया था और यह उनकी बौद्धिक संपदा है। प्रतिलिपि, वितरण (इंटरनेट पर अन्य साइटों और संसाधनों की प्रतिलिपि बनाकर) या कॉपीराइट धारक की पूर्व सहमति के बिना सूचना और वस्तुओं के किसी भी अन्य उपयोग को कानून द्वारा दंडनीय है। लेख की सामग्री प्राप्त करने और उन्हें उपयोग करने की अनुमति के लिए, कृपया देखें

 लाइव जर्नल
लाइव जर्नल फेसबुक
फेसबुक ट्विटर
ट्विटर