Použitie kovov alkalických zemín. Zlúčeniny alkalických kovov a ich použitie. Kvalitatívne reakcie s použitím iónov kovov alkalických zemín

Chemické vlastnosti alkalických kovov a kovov alkalických zemín sú podobné. Na vonkajšej energetickej úrovni alkalických kovov je jeden elektrón, kovy alkalických zemín - dva. Počas reakcií sa kovy ľahko rozchádzajú s valenčnými elektrónmi, čo ukazuje vlastnosti silného redukčného činidla.
Alkalické
Skupina I periodickej tabuľky zahŕňa alkalické kovy:
- lítium;
- sodík;
- draslík;
- rubídium;
- cézium;
- francium.

Obrázok: 1. Alkalické kovy.
Sú mäkké (dajú sa rezať nožom), majú nízku teplotu topenia a teplotu varu. Toto sú najaktívnejšie kovy.
Chemické vlastnosti alkalických kovov sú uvedené v tabuľke.
|
Reakcia |
Vlastnosti: |
Rovnica |
|
S kyslíkom |
Na vzduchu rýchlo oxiduje. Lítium vytvára oxid pri teplotách nad 200 ° C. Sodík tvorí zmes 80% peroxidu (R202) a 20% oxidu. Zvyšok kovov tvorí superoxidy (RO 2) |
4Li + 02 → 2Li20; 2Na + 02 → Na202; Rb + 02 → Rb02 |
|
Reaguje iba na lítium pri izbovej teplote |
6Li + N2 → 2Li 3 N |
|
|
S halogénmi |
Reakcia je prudká |
2Na + Cl2 → 2NaCl |
|
S nekovmi |
Pri zahriatí. Tvorte sulfidy, hydridy, fosfidy, silicídy. Iba lítium a sodík reagujú s uhlíkom a tvoria karbidy |
2K + S → K2S; 2Na + H2 → 2NaH; 2Cs + 5P → Cs2P5; Rb + Si → RbSi; 2Li + 2C → Li 2 C 2 |
|
Iba lítium reaguje pokojne. Sodík horí žltým plameňom. Draslík reaguje bleskovo. Cézium a rubídium explodujú |
2Na + 2H20 → 2NaOH + H2 - |
|
|
S kyselinami |
S kyselinou chlorovodíkovou, fosforečnou a zriedenými kyselinami sírovými reagujú výbušne. Pri reakcii s koncentrovanou kyselinou sírovou sa uvoľňuje sírovodík, s koncentrovanou kyselinou dusičnou vzniká oxid dusnatý (I), so zriedenou kyselinou dusičnou - dusíkom |
2Na + 2HCl → 2NaCl + H2; 8Na + 5H2S04 (konc.) → 4Na2S04 + H2S + 4H20; 8K + 10HNO3 (konc.) → 8KNO3 + N20 + 5H20; 10Na + 12HNO3 (zriedený) → N2 + 10NaNO3 + 6H20 |
|
S amoniakom |
Vytvorte amíny |
2Li + 2NH3 → 2LiNH2 + H2 |
Môže reagovať s organickými kyselinami a alkoholmi.
Alkalická zem
Kovy alkalických zemín sú v skupine II periodickej tabuľky:
- berýlium;
- horčík;
- vápnik;
- stroncium;
- bárium;
- rádium.

Obrázok: 2. Kovy alkalických zemín.
Na rozdiel od alkalických kovov sú tvrdšie. Nožom sa dá krájať iba stroncium. Najhustším kovom je rádium (5,5 g / cm 3).
Berýlium interaguje s kyslíkom iba pri zahriatí na 900 ° C. Nereaguje s vodíkom a vodou za žiadnych podmienok. Horčík oxiduje pri 650 ° C a pri vysokom tlaku reaguje s vodíkom.
V tabuľke sú uvedené hlavné chemické vlastnosti kovov alkalických zemín.
|
Reakcia |
Vlastnosti: |
Rovnica |
|
S kyslíkom |
Vytvorte oxidové filmy. Po zahriatí na 500 ° C sa spontánne zapáli |
2Mg + 02 → 2MgO |
|
S vodíkom |
Pri vysokých teplotách tvoria hydridy |
Sr + H2 → SrH2 |
|
S halogénmi a nekovmi |
Reagujte po zahriatí |
Be + Cl2 → BeCl2; Mg + S → MgS; 3Ca + 2P → Ca3P2; 3Ca + N2 → Ca3N2; Ba + 2C → BaC 2 |
|
Pri izbovej teplote |
Mg + 2H20 → Mg (OH) 2 + H2 |
|
|
S kyselinami |
Všetky kovy reagujú za vzniku solí |
4Ca + 10HNO3 (konc.) → 4Ca (NO3) 2 + N20 + 5H20 |
|
So zásadami |
Reaguje iba berýlium |
Be + 2NaOH + 2H20 → Na2 + H2 |
|
Striedanie |
Nahrádza menej aktívne kovy v oxidoch. Výnimkou je berýlium |
2Mg + ZrO2 → Zr + 2MgO |
Ióny alkalických kovov a kovov alkalických zemín v soliach sa dajú ľahko zistiť podľa zmeny farby plameňa. Sodné soli horia žltým plameňom, draslík - fialový, rubídium - červený, vápnik - tehlovočervený, bárium - žltozelený. Soli týchto kovov sa používajú na výrobu zábavnej pyrotechniky.

Obrázok: 3. Kvalitatívna odpoveď.
Čo sme sa naučili?
Alkalické kovy a kovy alkalických zemín sú aktívne prvky periodickej sústavy, ktoré reagujú s jednoduchými a zložitými látkami. Alkalické kovy sú mäkšie, prudko reagujú s vodou a halogénmi, ľahko oxidujú na vzduchu, tvoria oxidy, peroxidy, superoxidy, interagujú s kyselinami a amoniakom. Pri zahriatí reagujú s nekovmi. Kovy alkalických zemín reagujú s nekovmi, kyselinami, vodou. Berýlium nereaguje s vodíkom a vodou, ale reaguje s alkáliami a kyslíkom pri vysokých teplotách.
Test podľa témy
Posúdenie správy
Priemerné hodnotenie: 4.3. Celkový počet prijatých hodnotení: 113.
kovy alkalických zemín a chémia kovov alkalických zemínKovy alkalických zemín - chemické prvky 2. skupiny periodickej sústavy prvkov: vápnik, stroncium, bárium a rádium.
- 1 Fyzikálne vlastnosti
- 2 Chemické vlastnosti
- 2.1 Jednoduché látky
- 2.2 Oxidy
- 2.3 Hydroxidy
- 3 Byť v prírode
- 4 Biologická úloha
- 5 poznámok
Fyzikálne vlastnosti
Medzi kovy alkalických zemín patrí iba vápnik, stroncium, bárium a rádium, menej často horčík. Prvý prvok tejto podskupiny, berýlium, je vo väčšine svojich vlastností oveľa bližšie k hliníku ako k vyšším analógom skupiny, do ktorej patrí. Druhý prvok tejto skupiny, horčík, sa v niektorých ohľadoch významne líši od kovov alkalických zemín v rade chemických vlastností. Všetky kovy alkalických zemín sú šedé a tuhé látky pri izbovej teplote. Na rozdiel od alkalických kovov sú oveľa tvrdšie a väčšinou sa nerežú nožom (výnimkou je stroncium. Zvýšenie hustoty kovov alkalických zemín sa pozoruje až od vápnika. Najťažšie je rádium, ktoré je hustotou porovnateľné s germániom (ρ \u003d 5,5 g / cm3). ...
| Atómová číslo |
Názov, symbol |
Počet prírodných izotopov | Atómová hmotnosť | Ionizačná energia, kJ mol - 1 | Elektrónová afinita, kJ mol - 1 | EO | Kov. polomer, nm | Iónsky polomer, nm | tpl, ° C |
variť, ° C |
ρ, g / cm3 |
ΔHpl, kJ mol - 1 | ΔH var, kJ mol - 1 |
|---|---|---|---|---|---|---|---|---|---|---|---|---|---|
| 4 | Berýlium Be | 1 + 11a | 9,012182 | 898,8 | 0,19 | 1,57 | 0,169 | 0,034 | 1278 | 2970 | 1,848 | 12,21 | 309 |
| 12 | Horčík Mg | 3 + 19a | 24,305 | 737,3 | 0,32 | 1,31 | 0,24513 | 0,066 | 650 | 1105 | 1,737 | 9,2 | 131,8 |
| 20 | Vápnik Ca | 5 + 19a | 40,078 | 589,4 | 0,40 | 1,00 | 0,279 | 0,099 | 839 | 1484 | 1,55 | 9,20 | 153,6 |
| 38 | Strontium Sr | 4 + 35a | 87,62 | 549,0 | 1,51 | 0,95 | 0,304 | 0,112 | 769 | 1384 | 2,54 | 9,2 | 144 |
| 56 | Bárium Ba | 7 + 43a | 137,327 | 502,5 | 13,95 | 0,89 | 0,251 | 0,134 | 729 | 1637 | 3,5 | 7,66 | 142 |
| 88 | Rádium Ra | 46a | 226,0254 | 509,3 | - | 0,9 | 0,2574 | 0,143 | 700 | 1737 | 5,5 | 8,5 | 113 |
a rádioaktívne izotopy
Chemické vlastnosti
Kovy alkalických zemín majú elektronickú konfiguráciu úrovne vonkajšej energie ns² a sú to spolu s alkalickými kovmi aj s-prvky. Kovy kovov alkalických zemín, ktoré majú dva valenčné elektróny, ich ľahko rozdávajú a vo všetkých zlúčeninách majú oxidačný stav +2 (veľmi zriedka +1).
Chemická aktivita kovov alkalických zemín rastie so zvyšujúcim sa sériovým číslom. Berýlium v \u200b\u200bkompaktnej forme nereaguje ani s kyslíkom, ani s halogénmi ani pri červenom ohni (do 600 ° C je na reagovanie s kyslíkom a inými chalkogénmi potrebná ešte vyššia teplota, výnimkou je fluór). Horčík je chránený oxidovým filmom pri izbovej teplote a vyšších (do 650 ° C) teplotách a ďalej neoxiduje. Vápnik sa pomaly oxiduje dovnútra pri izbovej teplote (v prítomnosti vodnej pary) a horí pri miernom zahriatí na kyslík, ale je stabilný na suchom vzduchu pri izbovej teplote. Stroncium, bárium a rádium na vzduchu rýchlo oxidujú za vzniku zmesi oxidov a nitridov, takže sa podobne ako alkalické kovy a vápnik ukladajú pod vrstvou petroleja.
Na rozdiel od alkalických kovov tiež kovy alkalických zemín netvoria superoxidy a ozonidy.
Oxidy a hydroxidy kovov alkalických zemín majú tendenciu zlepšovať svoje základné vlastnosti so zvyšujúcim sa poradovým číslom.
Jednoduché látky
Berýlium reaguje so slabými a silnými kyslými roztokmi za vzniku solí:
avšak pasivuje sa studenou koncentrovanou kyselinou dusičnou.
Reakcia berýlia s vodnými roztokmi zásad je sprevádzaná vývojom vodíka a tvorbou hydroxyberyllátov:
Keď sa reakcia uskutočňuje s roztavenou zásadou pri 400 až 500 ° C, vytvárajú sa dioxoberylláty:
Horčík, vápnik, stroncium, bárium a rádium reagujú s vodou za vzniku zásad (s výnimkou horčíka, ktorý reaguje s vodou, iba ak sa do vody pridá horúci prášok horčíka):
Vápnik, stroncium, bárium a rádium tiež reagujú s vodíkom, dusíkom, bórom, uhlíkom a inými nekovmi za vzniku zodpovedajúcich binárnych zlúčenín:
Oxidy
Oxid berýlium je amfotérny oxid, ktorý sa rozpúšťa v koncentrovaných minerálnych kyselinách a zásadách za vzniku solí:
ale s menej silnými kyselinami a zásadami už reakcia nepokračuje.
Oxid horečnatý nereaguje so zriedenými a koncentrovanými zásadami, ale ľahko reaguje s kyselinami a vodou:
Oxidy vápnika, stroncia, bária a rádia sú zásadité oxidy, ktoré reagujú s vodou, silnými a slabými kyslými roztokmi a amfotérnymi oxidmi a hydroxidmi:
Hydroxidy
Hydroxid berýlium je amfotérny, pri reakcii so silnými zásadami vytvára beryláty, s kyselinami - berýlium soli kyselín:
Hydroxidy horčíka, vápnika, stroncia, bária a rádia sú zásady, pevnosť sa zvyšuje zo slabej na veľmi silnú, čo je najsilnejšia korozívna látka, ktorá prevyšuje aktivitu hydroxidu draselného. Dobre sa rozpúšťajú vo vode (okrem hydroxidov horečnatých a vápenatých). Vyznačujú sa reakciami s kyselinami a kyslými oxidmi a s amfoternými oxidmi a hydroxidmi:
Byť v prírode
Všetky kovy alkalických zemín sa nachádzajú (v rôznom množstve) v prírode. Kvôli vysokej chemickej aktivite sa všetky nevyskytujú v slobodnom stave. Najbežnejším kovom alkalických zemín je vápnik, ktorého množstvo je 3,38% (z hmotnosti zemskej kôry). Horčík je o niečo horší ako on, ktorého množstvo je 2,35% (z hmotnosti zemskej kôry). Baryum a stroncium sú tiež rozšírené v prírode, z toho 0,05% a 0,034% hmotnosti zemskej kôry. Berýlium je vzácny prvok, ktorého množstvo je 6 × 10−4% hmotnosti zemskej kôry. Pokiaľ ide o rádium, ktoré je rádioaktívne, je to najvzácnejšie zo všetkých kovov alkalických zemín, ale v uránových rudách sa vždy nachádza v malom množstve. najmä sa odtiaľ dá izolovať chemickými prostriedkami. Jeho obsah sa rovná 1,10−10% (z hmotnosti zemskej kôry).
Biologická úloha
Horčík sa nachádza v tkanivách zvierat a rastlín (chlorofyl), je kofaktorom mnohých enzymatických reakcií, je nevyhnutný pri syntéze ATP, podieľa sa na prenose nervových impulzov a aktívne sa používa v medicíne (bischofitoterapia atď.). Vápnik je bežná makroživina v rastlinách, zvieratách a ľuďoch. ľudské telo a iné stavovce, väčšina z nich je v kostre a zuboch. kosti obsahujú vápnik vo forme hydroxyapatitu. „Kostry“ väčšiny skupín bezstavovcov (huby, polypy koralov, mäkkýše atď.) Sú zložené z rôznych foriem uhličitanu vápenatého (vápna). Vápnikové ióny sa podieľajú na procesoch zrážania krvi a tiež slúžia ako jeden z univerzálnych sekundárnych poslov v bunkách a regulujú rôzne vnútrobunkové procesy - kontrakciu svalov, exocytózu vrátane vylučovania hormónov a neurotransmiterov. Stroncium môže nahradiť vápnik v prírodných tkanivách, pretože má podobné vlastnosti. v ľudskom tele je hmotnosť stroncia asi 1% hmotnosti vápnika.
V súčasnosti nie je nič známe o biologickej úlohe berýlia, bária a rádia. Všetky zlúčeniny bária a berýlia sú jedovaté. Rádium je extrémne rádiotoxické. správa sa v tele ako vápnik - asi 80% rádia, ktoré vstupuje do tela, sa nahromadí v kostnom tkanive. Vysoké koncentrácie rádia spôsobujú osteoporózu, spontánne zlomeniny kostí a zhubné nádory kostí a krvotvorného tkaniva. Nebezpečný je aj radón, plynný produkt rádioaktívneho rozpadu rádia.
Poznámky
- Podľa novej klasifikácie IUPAC. Podľa zastaranej klasifikácie patria do hlavnej podskupiny skupiny II periodickej tabuľky.
- Nomenklatúra anorganickej chémie. Odporúčania IUPAC 2005. - Medzinárodná únia čistej a aplikovanej chémie, 2005. - S. 51.
- Skupina 2 - Kovy alkalických zemín, Royal Society of Chemistry.
- Zlatý fond. Školská encyklopédia. Chémia. M.: Drop, 2003.
| Periodická tabuľka chemických prvkov D. I. Mendelejeva | ||||||||||||||||||||||||||||||||
|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|
| 1 | 2 | 3 | 4 | 5 | 6 | 7 | 8 | 9 | 10 | 11 | 12 | 13 | 14 | 15 | 16 | 17 | 18 | |||||||||||||||
| 1 | H | On | ||||||||||||||||||||||||||||||
| 2 | Li | Byť | B | C. | N | O | F | Ne | ||||||||||||||||||||||||
| 3 | Na | Mg | Al | Si | P | S | Cl | Ar | ||||||||||||||||||||||||
| 4 | K | Ca | Sc | Ti | V. | Cr | Mn | Fe | Spol | Ni | Cu | Zn | Ga | Ge | Ako | Se | Br | Kr | ||||||||||||||
| 5 | Rb | Sr | Y | Zr | Pozn | Mo | Tc | Ru | Rh | Pd | Ag | Cd | V | Sn | Sb | Te | Ja | Xe | ||||||||||||||
| 6 | Čs | Ba | La | Ce | Pr | Nd | Popoludnie | Sm | EÚ | Gd | Tb | D Y | Ho | Er | Tm | Yb | Lu | Hf | Ta | Ž | Re | Os | Ir | Pt | Au | Hg | Tl | Pb | Bi | Po | O | Rn |
| 7 | O | Ra | Ac | Th | Pa | U | Np | Pu | Am | Cm | Bk | Porov | Es | Fm | Md | Č. | Lr | Rf | Db | Sg | Bh | Hs | Mt. | Ds | Rg | Cn | Uut | Fl | Uup | Ľv | Uus | Uuo |
| 8 | Uue | Ubn | Ubu | Ubb | Ubt | Ubq | Ubp | Ubh | ||||||||||||||||||||||||
kovy alkalických zemín, kovy alkalických zemín a chémia kovov alkalických zemín, kovy alkalických zemín
Časť prvá. všeobecné charakteristikyIIA skupiny periodickej tabuľky prvkov.
V tejto skupine sú umiestnené tieto prvky: Be, Mg, Ca, Sr, Ba, Ra. Majú spoločnú elektronickú konfiguráciu: (n-1) p 6 ns 2, okrem Be 1s 2 2s 2. Vďaka tomu sa vlastnosti Be mierne líšia od vlastností podskupiny ako celku. Vlastnosti horčíka sa tiež líšia od vlastností podskupiny, ale v menšej miere. V sérii Ca - Sr - Ba - Ra sa vlastnosti menia postupne. Relatívna elektronegativita v sérii Be - Ra klesá, pretože so zväčšením atómovej veľkosti sa valenčné elektróny darujú ľahšie. Vlastnosti prvkov podskupiny IIA sú určené ľahkosťou vydávania dvoch ns elektrónov. V tomto prípade vzniknú ióny E 2+. Pri štúdiu röntgenovej difrakcie sa ukázalo, že v niektorých zlúčeninách vykazujú prvky podskupiny IIA univalenciu. Príkladom takýchto zlúčenín je EG, ktorý sa získa pridaním E k tavenine EG2. Všetky prvky tejto série sa v prírode nenachádzajú vo voľnom stave kvôli vysokej aktivite.
Druhá časť. Berýlium a horčík.
História berýlia
Zlúčeniny berýlia vo forme drahých kameňov sú známe už v staroveku. Ľudia dlho hľadali a rozvíjali ložiská modrých akvamarínov, zelených smaragdov, zelenožltého berylu a zlatého chrysoberylu. Ale až na konci 18. storočia chemici tušili, že beryl obsahuje nejaký nový neznámy prvok. V roku 1798 izoloval francúzsky chemik Lewis Nicolas Vauquelin oxid „La terree du beril“ z berylu, ktorý sa odlišoval od oxidu hlinitého. Tento oxid dodával soliam sladkú chuť, netvoril kamenec, rozpustil sa v roztoku uhličitanu amónneho a nevyzrážal sa šťavelanom draselným. Kovové berýlium prvýkrát získal v roku 1829 slávny nemecký vedec Weller a súčasne francúzsky vedec Bussy, ktorý prášok kovového berýlia získal redukciou chloridu berýlia kovovým draslíkom. Začiatok priemyselnej výroby sa datuje do 30. - 40. rokov. posledné storočie.
História horčíka
Názov prvku dostal podľa oblasti Magnesia v starovekom Grécku. Pri stavbe sa už dlho používali prírodné materiály obsahujúce magnézium a dolomit.
Prvé pokusy o izoláciu kovovej základne magnézia v čistej podobe sa uskutočnili na začiatku 19. storočia. slávny anglický fyzik a chemik Humphrey Davy (1778-1829) potom, čo podrobil elektrolýze tavenie hydroxidu draselného a lúhu sodného a získal kovový Na a K. Rozhodol sa pokúsiť podobným spôsobom uskutočniť rozklad oxidov kovov alkalických zemín a horčíka. Vo svojich počiatočných experimentoch prechádzal Davy prúdom cez mokré oxidy, ktoré im bránili v kontakte so vzduchom pomocou vrstvy oleja; v tomto prípade však boli kovy legované katódou a nedali sa oddeliť.
Davy vyskúšal mnoho rôznych metód, ale všetky boli z rôznych dôvodov neúspešné. Nakoniec mal v roku 1808 šťastie - zmiešal mokrú magnéziu s oxidom ortuťovým, hmotu položil na platinovú platňu a prešiel ňou prúdom; Amalgám sa preniesol do sklenenej skúmavky, zahrial sa na odstránenie ortuti a získal sa nový kov. Rovnakým spôsobom sa Davymu podarilo získať bárium, vápnik a stroncium. Priemyselná výroba horčíka elektrolytickou metódou sa začala v Nemecku na konci 19. storočia. Teoretické a experimentálne práce na výrobu horčíka elektrolytickou metódou u nás realizoval P.P. Fedotev; proces redukcie oxidu horečnatého kremíkom vo vákuu študoval P.F. Antipín.
Šírenie
Berýlium je jedným z nie veľmi bežných prvkov: jeho obsah v zemskej kôre je 0,0004% hmotn. %. Berýlium v \u200b\u200bprírode je v viazanom stave. Najdôležitejšie minerály berýlia: berýl - Be 3 Al 2 (SiO 3) 6, chrysoberyl - Be (AlO 2) 2 a fenakit - Be 2 SiO 4. Väčšina berýlia je nastriekaná ako nečistoty na minerály mnohých ďalších prvkov, najmä hliníka. Berýlium sa nachádza aj v hlbokých morských usadeninách a v popole niektorých druhov uhlia. Niektoré odrody berylu, zafarbené nečistotami v rôznych farbách, sú klasifikované ako drahé kamene. Sú to napríklad zelené smaragdy, modrozelené akvamaríny.
Horčík je jedným z najpočetnejších prvkov v zemskej kôre. Obsah horčíka je 1,4%. Medzi najdôležitejšie minerály patria predovšetkým uhličité uhličitany, ktoré tvoria obrovské masívy na pevnine a dokonca v celých pohoriach - magnezitMgC03 a dolomitMgCO3-CaCO3. Kolosálne ložiská iného ľahko rozpustného minerálu obsahujúceho horčík sú známe pod vrstvami rôznych naplavených hornín spolu s ložiskami kamennej soli - karnallitMgCl2-KCl-6H20. Okrem toho je horčík v mnohých mineráloch úzko spojený s oxidom kremičitým, ktorý vytvára napríklad olivín [(Mg, Fe) 2SiO4] a menej časté forsterit (Mg2Si04). Medzi ďalšie minerály obsahujúce horčík patria brucitMg (OH) 2 , kieseritMgS04 , epsoniteMgS04 -7H20 , kainitMgS04-KCl-3H20 . Na povrchu Zeme horčík ľahko vytvára vodnaté kremičitany (mastenec, azbest atď.), Príkladom ktorých je hadovitý 3MgO-2SiO 2 -2H 2 O. Zo známych minerálov asi 13% obsahuje horčík. Prírodné zlúčeniny horčíka sa však bežne vyskytujú v rozpustenej forme. Okrem rôznych minerálov a hornín je 0,13% horčíka vo forme MgCl 2 neustále obsiahnuté vo vodách oceánu (jeho zásoby sú tu nevyčerpateľné - asi 6 - 10 16 ton) a v slaných jazerách a prameňoch. Horčík je tiež súčasťou chlorofylu v množstve až 2% a pôsobí tu ako komplexotvorné činidlo. Celkový obsah tohto prvku v živej hmote Zeme sa odhaduje na asi 10 11 ton.
Príjem
Hlavnou (asi 70%) metódou výroby horčíka je elektrolýza roztaveného karnalitu alebo MgCl2 pod vrstvou tavidla, aby bol chránený pred oxidáciou. Tepelnou metódou na získanie horčíka (asi 30%) je redukcia vypáleného magnezitu alebo dolomitu. Berýliové koncentráty sa spracúvajú na oxid alebo hydroxid berýlinatý, z ktorého sa získava fluorid alebo chlorid. Pri získavaní kovového berýlia sa uskutočňuje elektrolýza taveniny BeCl2 (50% hmotn.) A NaCl. Táto zmes má teplotu topenia 300 ° C oproti 400 ° C pre čistý BeCl2. Berýlium sa tiež získava horčíkom alebo alumotermicky pri teplote 1 000 - 1 200 ° C z Na2: Na2 + 2Mg \u003d Be + 2Na + MgF2. Vysoko čisté berýlium (hlavne pre jadrový priemysel) sa získava zónovým tavením, vákuovou destiláciou a elektrolytickou rafináciou.
Vlastnosti:
Berýlium je „čistý“ prvok. Horčík sa prirodzene vyskytuje vo forme troch stabilných izotopov: 24 Mg (78,60%), 25 Mg (10,11%) a 26 Mg (11,29%). Izotopy s hmotnosťou 23, 27 a 28 boli získané umelo.
Berýlium má atómové číslo 4 a atómovú hmotnosť 9,0122. Je v druhej perióde periodického systému a vedie hlavnú podskupinu skupiny 2. Elektronická štruktúra atómu berýlia je 1s 2 2s 2. Počas chemickej interakcie sa excituje atóm berýlia (vyžaduje si cenu 63 kcal / g × atóm) a jeden z elektrónov 2s sa prenesie na 2p-orbitál, čo určuje špecifickosť chémie berýlia: môže vykazovať maximálnu kovalenciu 4 a tvoriť 2 väzby mechanizmom výmeny, a 2 pre darcu-príjemcu. Berýlium zaujíma jednu z horných pozícií na krivke ionizačného potenciálu. Ten zodpovedá jeho malému polomeru a charakterizuje berýlium ako prvok, ktorý nie je zvlášť ochotný darovať svoje elektróny, čo určuje predovšetkým nízky stupeň chemickej aktivity prvku. Z hľadiska elektronegativity možno berýlium považovať za typický prechodný prvok medzi elektropozitívnymi atómami kovov, ktoré ľahko darujú svoje elektróny, a typickými komplexotvornými látkami, ktoré majú tendenciu vytvárať kovalentnú väzbu. Berýlium vykazuje diagonálnu analógiu s hliníkom vo väčšej miere ako LicMg a je kainosymetrickým prvkom. Berýlium a jeho zlúčeniny sú vysoko toxické. MPC vo vzduchu - 2 μg / m 3.
V periodickej tabuľke prvkov sa horčík nachádza v hlavnej podskupine skupiny II; poradové číslo horčíka je 12, atómová hmotnosť 24,312. Elektronická konfigurácia excitovaného atómu je 1s 2 2s 2 2p 6 3s 2; štruktúra vonkajších elektrónových škrupín atómu Mg (3s 2) zodpovedá jeho nulovému valenčnému stavu. Budenie na bivalentné 3s 1 3p 1 vyžaduje náklady 62 kcal / g-atóm. Ionizačné potenciály horčíka sú nižšie ako potenciály berýlia, preto sa zlúčeniny horčíka vyznačujú vyšším podielom väzbovej ionicity. Z hľadiska komplexotvornej schopnosti je horčík tiež horší ako berýlium. Interakcia s prvkami skupiny IIIB s nedokončenými d-mušľami má niektoré zvláštnosti. Táto skupina zahŕňa Sc, Y, Ln a Th. Tieto prvky tvoria s horčíkom množstvo prechodných fáz a dobre sa v nich rozpúšťajú v tekutom stave. Stavové diagramy zmesí týchto prvkov s horčíkom majú eutektický charakter. Rozpustnosť týchto prvkov v horčíku v tuhom stave nie je veľká (2 - 5% hmotnostných). Pokiaľ ide o alkalické zeminy a najmä alkalické kovy, horčík netvorí významnú oblasť rozpustnosti v tuhom stave, čo je spojené s veľkým rozdielom v atómových polomeroch. Výnimkou je lítium, ktorého atómový polomer sa líši od atómového polomeru horčíka o 2%. Systémy horčíka s meďou, striebrom a zlatom sú eutektického typu. Rozpustnosť striebra pri eutektickej teplote –16% hmotnostných.
Fyzikálne vlastnosti
Berýlium - strieborno-biely kov. Dosť tvrdé a krehké. Má diamagnetické vlastnosti. Na vzduchu je pokrytý tenkým oxidovým filmom, ktorý dodáva kovu šedú, matnú farbu a chráni ho pred ďalšou koróziou. Stlačiteľnosť berýlia je veľmi nízka. Najmenej zo všetkých kovov (17-krát menej ako Al) inhibuje röntgenové lúče. Kryštalizuje v štruktúre hcp s periódami a \u003d 0,228 nm a c \u003d 0,358 nm, CN \u003d 6. Pri 1254 ° C sa hexagonálna a-modifikácia transformuje na kubický b. Berýlium vytvára eutektické zliatiny s Al a Si.
UMIESTNENIE V PRÍRODE
Zemská kôra obsahuje berýlium - 0,00053%, horčík - 1,95%, vápnik - 3,38%, stroncium - 0,014%, bárium - 0,026%, rádium - umelý prvok.
Nachádza sa v prírode iba vo forme zlúčenín - kremičitany, hlinitokremičitany, uhličitany, fosfáty, sírany atď.
ZÍSKAVANIE
1. Berýlium sa získava redukciou fluoridu:
BeF 2 + Mg t ˚ C → Be + MgF 2
2. Bárium sa získava redukciou oxidu:
3BaO + 2Al t ˚ C → 3Ba + Al203
3. Zvyšok kovov sa získava elektrolýzou chloridových tavenín:
Pretože Pretože kovy tejto podskupiny sú silnými redukčnými činidlami, je možné ich získať iba elektrolýzou roztavených solí. V prípade Ca sa zvyčajne používa CaCl2 (s prídavkom CaF 2 na zníženie teploty topenia)
CaCl2 \u003d Ca + Cl2
FYZIKÁLNE VLASTNOSTI
Kovy alkalických zemín (v porovnaní s alkalickými kovmi) majú vyššiu t ° pl. a t ° balíky, hustota a tvrdosť.
APLIKÁCIA
| Berýlium (amfoterín) | Horčík | Ca, Sr, Ba, Ra |
| 1. Výroba tepelne tieniacich konštrukcií pre vesmír. lode (tepelná odolnosť, tepelná kapacita berýlia) 2. Bronzové berýlium (ľahkosť, tvrdosť, tepelná odolnosť, antikorózna ochrana zliatin, pevnosť v ťahu vyššia ako oceľ, možno stočiť do pásov s hrúbkou 0,1 mm) 3. V jadrových reaktoroch, v röntgenovom žiarení, v rádiovej elektronike 4. Byť zliatinou „Ni, W - Švajčiarsko vyrába pružiny hodiniek. Ale Be je krehký, jedovatý a veľmi drahý | 1. Získavanie kovov - horčík - termálne (titán, urán, zirkónium atď.) 2. Získanie ultraľahkých zliatin (výroba lietadiel, automobilov) 3. V organickej syntéze 4. Na výrobu svetelných a zápalných rakiet. | 1. Výroba zliatin olova a kadmia potrebných na výrobu ložísk. 2. Stroncium je redukčné činidlo pri výrobe uránu. Fosfory sú soli stroncia. 3. Používa sa ako getre, látky na vytváranie vákua v elektrických prístrojoch. Vápnik získavajúci vzácne kovy je súčasťou zliatin. Getar bárnatý v katódových trubiciach. Rádiová röntgenová diagnostika, výskumné práce. |
CHEMICKÉ VLASTNOSTI
1. Veľmi reaktívne, silné redukčné činidlá. Aktivita kovov a ich redukčná schopnosť sa zvyšujú v tomto poradí: Be - Mg - Ca - Sr - Ba
2. Majú oxidačný stav +2.
3. Reagujte s vodou pri teplote miestnosti (okrem Be), aby sa uvoľnil vodík.
4. S vodíkom tvoria hydridy podobné soli EH2.
5. Oxidy majú všeobecný vzorec EO. Tendencia k tvorbe peroxidov je menej výrazná ako u alkalických kovov.
Reakcia s vodou.
Za normálnych podmienok je povrch Be a Mg pokrytý inertným oxidovým filmom, takže sú odolné voči vode, ale pomocou horúcej vody tvorí horčík bázu Mg (OH) 2.
Na rozdiel od toho sa Ca, Sr a Ba rozpúšťajú vo vode za vzniku hydroxidov, ktoré sú silnými zásadami:
Be + H20 → BeO + H2
Ca + 2H20 → Ca (OH) 2 + H2
Reakcia s kyslíkom.
Všetky kovy tvoria oxidy RO, bárium peroxid - BaO 2:
2Mg + 02 → 2MgO
Ba + O 2 → BaO 2
3. Binárne zlúčeniny sa tvoria s inými nekovmi:
Be + Cl2 → BeCl2 (halogenidy)
Ba + S → BaS (sulfidy)
3Mg + N2 → Mg3N2 (nitridy)
Ca + H 2 → CaH 2 (hydridy)
Ca + 2C → CaC 2 (karbidy)
3Ba + 2P → Ba 3 P 2 (fosfidy)
Berýlium a horčík reagujú s nekovmi pomerne pomaly.
4. Všetky kovy sa rozpúšťajú v kyselinách:
Ca + 2HCl → CaCl2 + H2
Mg + H2S04 (zried.) → MgS04 + H2
Berýlium sa tiež rozpúšťa vo vodných roztokoch zásad:
Be + 2NaOH + 2H20 → Na2 + H2
5. Kvalitatívna reakcia na katióny kovov alkalických zemín - sfarbenie plameňa v nasledujúcich farbách:
Ca 2+ - tmavo oranžová
Sr 2+ - tmavočervená
Ba 2+ - svetlozelená
Katión Ba 2+ sa zvyčajne otvára výmennou reakciou s kyselinou sírovou alebo jej soľami:
BaCl2 + H2S04 → BaSO4 ↓ + 2HCl
Ba 2+ + SO 4 2- → BaSO 4 ↓
Síran bárnatý je biela zrazenina, nerozpustná v minerálnych kyselinách.
Oxidy kovov alkalických zemín
Príjem
1) Oxidácia kovov (okrem Ba, ktorá vytvára peroxid)
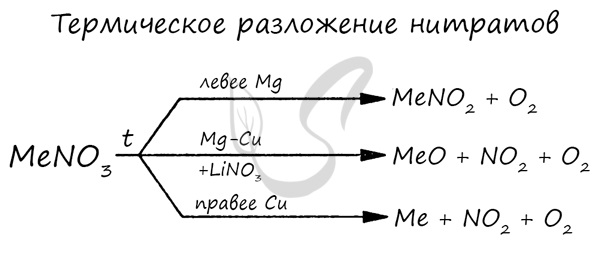
2) Tepelný rozklad dusičnanov alebo uhličitanov
CaCO 3 t ˚ C → CaO + CO2
2Mg (NO3) 2 t˚C → 2MgO + 4NO2 + O2
Chemické vlastnosti
Typické zásadité oxidy. Reagujte s vodou (okrem BeO a MgO), oxidmi kyselín a kyselinami
CaO + H20 → Ca (OH) 2
3CaO + P205 → Ca3 (PO4) 2
BeO + 2HNO3 → Be (NO3) 2 + H20
BeO - amfoterný oxid, rozpustný v zásadách:
BeO + 2NaOH + H20 → Na2
Hydroxidy kovov alkalických zemín R (OH) 2
Príjem
Reakcie kovov alkalických zemín alebo ich oxidov s vodou:
Ba + 2H20 → Ba (OH) 2 + H2
CaO (nehasené vápno) + H20 → Ca (OH) 2 (hasené vápno)
Chemické vlastnosti
Hydroxidy R (OH) 2 sú biele kryštalické látky, menej rozpustné vo vode ako hydroxidy alkalických kovov ( rozpustnosť hydroxidov klesá so znižujúcim sa sériovým číslom; Be (OH) 2 - nerozpustný vo vode, rozpustný v zásadách). Zásaditosť R (OH) 2 rastie so zvyšujúcim sa atómovým číslom:
Be (OH) 2 - amfoterný hydroxid
Mg (OH) 2 - slabá báza
Ca (OH) 2 - zásada
ďalšie hydroxidy sú silné zásady (zásady).
1) Reakcie s kyslými oxidmi:
Ca (OH) 2 + CO 2 → CaCO 3 ↓ + H 2 O! Kvalitatívna odpoveď na oxid uhličitý
Ba (OH) 2 + S02 → BaSO3 ↓ + H20
2) Reakcie s kyselinami:
Ba (OH) 2 + 2HNO3 → Ba (NO3) 2 + 2H20
3) Reakcie výmeny so soľami:
Ba (OH) 2 + K2S04 → BaSO4 ↓ + 2KOH
4) Reakcia hydroxidu berýlia s alkáliami:
Buďte (OH) 2 + 2NaOH → Na2
Tvrdosť vody
Prírodná voda obsahujúca ióny Ca 2+ a Mg 2+ sa nazýva tvrdá. Keď sa z varenej tvrdej vody vytvorí vodný kameň, potravinárske výrobky sa v nej nerozvaria; čistiace prostriedky nepenia.
Uhličitanová (dočasná) tvrdosť v dôsledku prítomnosti hydrogenuhličitanov vápenatých a horečnatých vo vode, nekarbonátová (stála) tvrdosť - chloridy a sírany.
Celková tvrdosť vody sa považuje za sumu uhličitanu a ne-uhličitanu.
Odstránenie tuhosti voda sa uskutočňuje vyzrážaním iónov Ca 2+ a Mg 2+ z roztoku
Medzi kovy alkalických zemín patria kovy skupiny IIa: berýlium, horčík, vápnik, stroncium, bárium a rádium. Vyznačujú sa ľahkosťou, mäkkosťou a silnou reaktivitou.
všeobecné charakteristiky
Od Be po Ra (v periodickej tabuľke zhora nadol) sa zvyšuje: atómový polomer, kovový, zásaditý, redukčné vlastnosti, reaktivita. Znižuje elektronegativitu, ionizačnú energiu, elektrónovú afinitu.
Elektronické konfigurácie týchto prvkov sú podobné, pretože sú v rovnakej skupine (hlavná podskupina!). Všeobecný vzorec je ns 2:
- Buďte - 2 s 2
- Mg - 3 s 2
- Ca - 4 s 2
- Sr - 5s 2
- Ba - 6s 2
- Ra - 7 s 2
Prírodné zlúčeniny
V prírode sa kovy alkalických zemín nachádzajú v nasledujúcich zlúčeninách:
- Be - BeO * Al 2 O 3 * 6SiO 2 - beryl
- Mg - MgCO 3 - magnezit, MgO * Al 2 O 3 - spinel, 2MgO * SiO 2 - olivín
- Ca - CaCO 3 - krieda, mramor, vápenec, kalcit, CaSO 4 * 2H 2 O - sadra, CaF 2 - fluorit

Príjem
Ide o aktívne kovy, ktoré nie je možné získať elektrolýzou roztoku. Na ich získanie sa používa elektrolýza tavenín, aluminotermia a ich vytesňovanie zo solí inými aktívnejšími kovmi.
MgCl2 → (t) Mg + Cl2 (elektrolýza v tavenine)
CaO + Al → Al 2 O 3 + Ca (aluminotermia je metóda výroby kovov redukciou ich oxidov s hliníkom)
MgBr 2 + Ca → CaBr 2 + Mg

Chemické vlastnosti

Oxidy kovov alkalických zemín
Majú všeobecný vzorec RO, napríklad: MgO, CaO, BaO.
Príjem
Oxidy kovov alkalických zemín možno získať rozkladom uhličitanov a dusičnanov:
MgC03 → (t) MgO + C02
Ca (N03) 2 → (t) CaO + 02 + N02
Chemické vlastnosti
Vykazujú hlavne základné vlastnosti, všetky okrem BeO - amfoterného oxidu.

Hydroxidy kovov alkalických zemín
Vykazujú základné vlastnosti, s výnimkou hydroxidu berýlia, amfoterného hydroxidu.
Príjem
Hydroxidy sa získavajú reakciou zodpovedajúceho oxidu kovu a vody (všetky okrem Be (OH) 2)
CaO + H20 → Ca (OH) 2
Chemické vlastnosti
Základné vlastnosti väčšiny hydroxidov sú priaznivé pre reakcie s kyselinami a kyslými oxidmi.
Ba (OH) 2 + H2S04 → BaSO4 ↓ + H20
Ca (OH) 2 + H20 + C02 → Ca (HCO3) 2 + H20
Ca (HCO3) 2 + Ca (OH) 2 → CaCO3 + H20 + CO2
Ca (OH) 2 + C02 → CaCO3 ↓ + H20

K reakcii so soľami (a nielen) dochádza, ak je soľ rozpustná a v dôsledku uvoľňovania reakčného plynu sa tvorí zrazenina alebo slabý elektrolyt (voda).
Ba (OH) 2 + Na2S04 → BaSO4 ↓ + NaOH
Hydroxid berylnatý je amfotérny: vykazuje dvojité vlastnosti a reaguje s kyselinami aj zásadami.
Be (OH) 2 + HCl → BeCl2 + H20
Buďte (OH) 2 + NaOH → Na2
Tvrdosť vody je kombináciou vlastností vody, v závislosti od jej prítomnosti predovšetkým vápenatých a horečnatých solí: hydrouhličitany, sírany a chloridy.
Rozlišujte medzi dočasnou (uhličitanovou) a trvalou (ne-uhličitanovou) tvrdosťou.

Pravdepodobne doma tvrdo bojujete s vodou, dovolím si tvrdiť - každý deň. Dočasná tvrdosť vody sa eliminuje obyčajným varením vody v kanvici a vápno na jej stenách - CaCO 3 - je nespochybniteľným dôkazom odstránenia tvrdosti:
Ca (HCO3) 2 → CaCO3 ↓ + C02 + H20
Dočasnú tvrdosť je tiež možné vylúčiť pridaním Na2C03 do vody:
Ca (HCO3) 2 + Na2C03 → CaCO3 ↓ + NaHCO3
Je zbytočné bojovať s konštantnou tvrdosťou varom: síry a chloridy sa počas varu nezrážajú. Konštantná tvrdosť vody sa eliminuje pridaním Na2C03 do vody:
CaCl2 + Na2C03 → CaCO3 ↓ + NaCl
MgSO 4 + Na 2 CO 3 + H 2 O → 2 CO 3 ↓ + CO 2 + Na 2 SO 4
Tvrdosť vody sa dá určiť pomocou rôznych testov. Príliš vysoká tvrdosť vody vedie k rýchlemu tvorbe vodného kameňa na stenách kotlov, potrubí, rýchlovarnej kanvice.

© Bellevich Jurij Sergejevič
Tento článok napísal Jurij Sergejevič Bellevič a je jeho duševným vlastníctvom. Kopírovanie, distribúcia (vrátane kopírovania na iné stránky a zdroje na internete) alebo akékoľvek iné použitie informácií a objektov bez predchádzajúceho súhlasu držiteľa autorských práv je trestné podľa zákona. Materiály k článku a povolenie na ich použitie nájdete v časti
- História vzniku románu
- Ako nainštalovať ruštinu na iPhone
- Vyšetrovacie kódy qr strážnych psov
- Widescreen Fix - širokouhlé rozlíšenie pre Need for Speed: Most Wanted (2005) Mod pre nfs, ktoré sú najžiadanejšie pre rozlíšenie
- Ako pridať alebo odstrániť jazyk v systéme Windows XP, povoliť pravopis zľava a hieroglyfy
- Ako pridať jazyk na panel jazykov Windows
- Ako môžem pridať jazyk na panel jazykov v systéme Windows?

 Živý denník
Živý denník Facebook
Facebook Twitter
Twitter