Использование щелочноземельных металлов. Соединения щелочных металлов и их применение. Качественные реакции с использованием ионов щелочноземельных металлов

Химические свойства щелочных и щелочноземельных металлов схожи. На внешнем энергетическом уровне щелочных металлов находится один электрон, щелочноземельных - два. При реакциях металлы легко расстаются с валентными электронами, проявляя свойства сильного восстановителя.
Щелочные
В I группу периодической таблицы входят щелочные металлы:
- литий;
- натрий;
- калий;
- рубидий;
- цезий;
- франций.

Рис. 1. Щелочные металлы.
Они отличаются мягкостью (можно разрезать ножом), низкими температурами плавления и кипения. Это наиболее активные металлы.
Химические свойства щелочных металлов представлены в таблице.
|
Реакция |
Особенности |
Уравнение |
|
С кислородом |
Быстро окисляются на воздухе. Литий образует оксид при температуре выше 200°C. Натрий образует смесь - 80 % пероксида (R 2 O 2) и 20 % оксида. Остальные металлы образуют надпероксиды (RO 2) |
4Li + O 2 → 2Li 2 O; 2Na + О 2 → Na 2 O 2 ; Rb + O 2 → RbO 2 |
|
Реагирует только литий при комнатной температуре |
6Li + N 2 → 2Li 3 N |
|
|
С галогенами |
Реакция проходит бурно |
2Na + Cl 2 → 2NaCl |
|
С неметаллами |
При нагревании. Образуют сульфиды, гидриды, фосфиды, силициды. С углеродом реагируют только литий и натрий, образуя карбиды |
2K + S → K 2 S; 2Na + H 2 → 2NaH; 2Cs + 5P → Cs 2 P 5 ; Rb + Si → RbSi; 2Li + 2C → Li 2 C 2 |
|
Спокойно реагирует только литий. Натрий горит жёлтым пламенем. Калий реагирует со вспышкой. Цезий и рубидий взрываются |
2Na + 2H 2 O → 2NaOH + H 2 - |
|
|
С кислотами |
С соляной, фосфорной, разбавленной серной кислотами реагируют с взрывом. При реакции с концентрированной серной кислотой выделяется сероводород, с концентрированной азотной кислотой образует оксид азота (I), с разбавленной азотной кислотой - азот |
2Na + 2HCl → 2NaCl + H 2 ; 8Na + 5H 2 SO 4 (конц) → 4Na 2 SO 4 + H 2 S + 4H 2 O; 8K + 10HNO 3 (конц) → 8KNO 3 + N 2 O + 5H 2 O; 10Na + 12HNO 3 (разб) → N 2 + 10NaNO 3 + 6H 2 O |
|
С аммиаком |
Образуют амины |
2Li + 2NH 3 → 2LiNH 2 + H 2 |
Могут реагировать с органическими кислотами и спиртами.
Щелочноземельные
Во II группе таблицы Менделеева находятся щелочноземельные металлы:
- бериллий;
- магний;
- кальций;
- стронций;
- барий;
- радий.

Рис. 2. Щелочноземельные металлы.
В отличие от щелочных металлов они более твёрдые. Ножом можно разрезать только стронций. Наиболее плотный металл - радий (5,5 г/см 3).
Бериллий взаимодействует с кислородом только при нагревании до 900°С. С водородом и водой не реагирует при любых условиях. Магний окисляется при температуре 650°С и взаимодействует с водородом под высоким давлением.
В таблице отражены основные химические свойства щелочноземельных металлов.
|
Реакция |
Особенности |
Уравнение |
|
С кислородом |
Образуют оксидные плёнки. При нагревании до 500°С самовоспламеняются |
2Mg + O 2 → 2MgO |
|
С водородом |
При высокой температуре образуют гидриды |
Sr + H 2 → SrH 2 |
|
С галогенами и неметаллами |
Реагируют при нагревании |
Be + Cl 2 → BeCl 2 ; Mg + S → MgS; 3Ca + 2P → Ca 3 P 2 ; 3Ca + N 2 → Ca 3 N 2 ; Ba + 2C → BaC 2 |
|
При комнатной температуре |
Mg + 2H 2 O → Mg(OH) 2 + H 2 |
|
|
С кислотами |
Реагируют все металлы с образованием солей |
4Ca + 10HNO 3 (конц.) → 4Ca(NO 3) 2 + N 2 O + 5H 2 O |
|
Со щелочами |
Реагирует только бериллий |
Be + 2NaOH + 2H 2 O → Na 2 + H 2 |
|
Замещение |
Замещают менее активные металлы в оксидах. Исключение - бериллий |
2Mg + ZrO 2 → Zr + 2MgO |
Ионы щелочных и щелочноземельных металлов в солях легко обнаружить по изменению цвета пламени. Соли натрия горят жёлтым пламенем, калия - фиолетовым, рубидия - красным, кальция - кирпично-красным, бария - жёлто-зелёным. Соли этих металлов используют для создания фейерверков.

Рис. 3. Качественная реакция.
Что мы узнали?
Щелочные и щелочноземельные металлы - активные элементы периодической таблицы, вступающие в реакции с простыми и сложными веществами. Щелочные металлы более мягкие, бурно реагируют с водой и галогенами, легко окисляются на воздухе, образуя оксиды, пероксиды, надпероксиды, взаимодействуют с кислотами и аммиаком. При нагревании вступают в реакцию с неметаллами. Щелочноземельные металлы реагируют с неметаллами, кислотами, водой. Бериллий не взаимодействует с водородом и водой, но реагирует со щелочами и с кислородом при высокой температуре.
Тест по теме
Оценка доклада
Средняя оценка: 4.3 . Всего получено оценок: 113.
щёлочноземельные металлы и, щёлочноземельные металлы химияЩёлочноземе́льные мета́ллы - химические элементы 2-й группы периодической таблицы элементов: кальций, стронций, барий и радий.
- 1 Физические свойства
- 2 Химические свойства
- 2.1 Простые вещества
- 2.2 Оксиды
- 2.3 Гидроксиды
- 3 Нахождение в природе
- 4 Биологическая роль
- 5 Примечания
Физические свойства
К щёлочноземельным металлам относят только кальций, стронций, барий и радий, реже магний. Первый элемент этой подгруппы, бериллий, по большинству свойств гораздо ближе к алюминию, чем к высшим аналогами группы, в которую он входит. Второй элемент этой группы, магний, в некоторых отношениях значительно отличается от щелочноземельных металлов по ряду химических свойств. Все щёлочноземельные металлы серые, твёрдые при комнатной температуре вещества. отличие от щелочных металлов, они существенно более твёрдые, и ножом преимущественно не режутся (исключение - стронций. Рост плотности щёлочноземельных металлов наблюдается только начиная с кальция. Самый тяжёлый - радий, по плотности сравнимый с германием (ρ= 5,5 г/см3).
| Атомный номер |
Название, символ |
Число природных изотопов | Атомная масса | Энергия ионизации, кДж моль−1 | Сродство к электрону, кДж моль−1 | ЭО | Металл. радиус, нм | Ионный радиус, нм | tпл, °C |
tкип, °C |
ρ, г/см³ |
ΔHпл, кДж моль−1 | ΔHкип, кДж моль−1 |
|---|---|---|---|---|---|---|---|---|---|---|---|---|---|
| 4 | Бериллий Be | 1+11а | 9,012182 | 898,8 | 0,19 | 1,57 | 0,169 | 0,034 | 1278 | 2970 | 1,848 | 12,21 | 309 |
| 12 | Магний Mg | 3+19а | 24,305 | 737,3 | 0,32 | 1,31 | 0,24513 | 0,066 | 650 | 1105 | 1,737 | 9,2 | 131,8 |
| 20 | Кальций Ca | 5+19а | 40,078 | 589,4 | 0,40 | 1,00 | 0,279 | 0,099 | 839 | 1484 | 1,55 | 9,20 | 153,6 |
| 38 | Стронций Sr | 4+35а | 87,62 | 549,0 | 1,51 | 0,95 | 0,304 | 0,112 | 769 | 1384 | 2,54 | 9,2 | 144 |
| 56 | Барий Ba | 7+43а | 137,327 | 502,5 | 13,95 | 0,89 | 0,251 | 0,134 | 729 | 1637 | 3,5 | 7,66 | 142 |
| 88 | Радий Ra | 46а | 226,0254 | 509,3 | - | 0,9 | 0,2574 | 0,143 | 700 | 1737 | 5,5 | 8,5 | 113 |
а Радиоактивные изотопы
Химические свойства
Щёлочноземельные металлы имеют электронную конфигурацию внешнего энергетического уровня ns², и являются s-элементами, наряду с щелочными металлами. Имея два валентных электрона, щёлочноземельные металлы легко их отдают, и во всех соединениях имеют степень окисления +2 (очень редко +1).
Химическая активность щёлочноземельных металлов растёт с ростом порядкового номера. Бериллий в компактном виде не реагирует ни с кислородом, ни с галогенами даже при температуре красного каления (до 600 °C, для реакции с кислородом и другими халькогенами нужна ещё более высокая температура, фтор - исключение). Магний защищён оксидной плёнкой при комнатной температуре и более высоких (до 650 °C) температурах и не окисляется дальше. Кальций медленно окисляется и при комнатной температуре вглубь (в присутствии водяных паров), и сгорает при небольшом нагревании в кислороде, но устойчив в сухом воздухе при комнатной температуре. Стронций, барий и радий быстро окисляются на воздухе, давая смесь оксидов и нитридов, поэтому их, подобно щелочным металлам и кальцию, хранят под слоем керосина.
Также, в отличие от щелочных металлов, щелочноземельные металлы не образуют надпероксиды и озониды.
Оксиды и гидроксиды щёлочноземельных металлов имеют тенденцию к усилению основных свойств с ростом порядкового номера.
Простые вещества
Бериллий реагирует со слабыми и сильными растворами кислот с образованием солей:
однако пассивируется холодной концентрированной азотной кислотой.
Реакция бериллия с водными растворами щелочей сопровождается выделением водорода и образованием гидроксобериллатов:
При проведении реакции с расплавом щелочи при 400-500 °C образуются диоксобериллаты:
Магний, кальций, стронций, барий и радий реагируют с водой с образованием щелочей (кроме магния, реакция которого с водой происходит только при внесении раскалённого порошка магния в воду):
Также, кальций, стронций, барий и радий реагируют с водородом, азотом, бором, углеродом и другими неметаллами с образованием соответствующих бинарных соединений:
Оксиды
Оксид бериллия - амфотерный оксид, растворяется в концентрированных минеральных кислотах и щелочах с образованием солей:
но с менее сильными кислотами и основаниями реакция уже не идет.
Оксид магния не реагирует с разбавленными и концентрированными основаниями, но легко реагирует с кислотами и водой:
Оксиды кальция, стронция, бария и радия - основные оксиды, реагируют с водой, сильными и слабыми растворами кислот и амфотерными оксидами и гидроксидами:
Гидроксиды
Гидроксид бериллия амфотерен, при реакциях с сильными основаниями образует бериллаты, с кислотами - бериллиевые соли кислот:
Гидроксиды магния, кальция, стронция, бария и радия - основания, сила увеличивается от слабого до очень сильного, являющегося сильнейшим коррозионным веществом, по активности превышающим гидроксид калия. Хорошо растворяются в воде (кроме гидроксидов магния и кальция). Для них характерны реакции с кислотами и кислотными оксидами и с амфотерными оксидами и гидроксидами:
Нахождение в природе
Все щёлочноземельные металлы имеются (в разных количествах) в природе. Ввиду своей высокой химической активности все они в свободном состоянии не встречаются. Самым распространённым щёлочноземельным металлом является кальций, количество которого равно 3,38 % (от массы земной коры). Немногим ему уступает магний, количество которого равно 2,35 % (от массы земной коры). Распространены в природе также барий и стронций, которых соответственно 0,05 и 0,034 % от массы земной коры. Бериллий является редким элементом, количество которого составляет 6·10−4% от массы земной коры. Что касается радия, который радиоактивен, то это самый редкий из всех щёлочноземельных металлов, но он в небольшом количестве всегда содержится в уранновых рудах. частности, он может быть выделен оттуда химическим путём. Его содержание равно 1·10−10% (от массы земной коры).
Биологическая роль
Магний содержится в тканях животных и растений (хлорофилл), является кофактором многих ферметативных реакций, необходим при синтезе АТФ, участвует в передаче нервных импульсов, активно применяется в медицине (бишофитотерапия и др.). Кальций - распространенный макроэлемент в организме растений, животных и человека. организме человека и других позвоночных большая его часть находится в скелете и зубах. костях кальций содержится в виде гидроксиапатита. Из различных форм карбоната кальция (извести) состоят «скелеты» большинства групп беспозвоночных (губки, коралловые полипы, моллюски и др.). Ионы кальция участвуют в процессах свертывания крови, а также служат одним из универсальных вторичных посредников внутри клеток и регулируют самые разные внутриклеточные процессы - мышечное сокращение, экзоцитоз, в том числе секрецию гормонов и нейромедиаторов. Стронций может замещать кальций в природных тканях, так как схож с ним по свойствам. организме человека масса стронция составляет около 1 % от массы кальция.
На данный момент о биологической роли бериллия, бария и радия ничего не известно. Все соединения бария и бериллия ядовиты. Радий чрезвычайно радиотоксичен. организме он ведёт себя подобно кальцию - около 80 % поступившего в организм радия накапливается в костной ткани. Большие концентрации радия вызывают остеопороз, самопроизвольные переломы костей и злокачественные опухоли костей и кроветворной ткани. Опасность представляет также радон - газообразный радиоактивный продукт распада радия.
Примечания
- По новой классификации ИЮПАК. По устаревшей классификации относятся к главной подгруппе II группы периодической таблицы.
- Nomenclature of Inorganic Chemistry. IUPAC Recommendations 2005. - International Union of Pure and Applied Chemistry, 2005. - P. 51.
- Group 2 - Alkaline Earth Metals, Royal Society of Chemistry.
- Золотой фонд. Школьная энциклопедия. Химия. М.: Дрофа, 2003.
| Периодическая система химических элементов Д. И. Менделеева | ||||||||||||||||||||||||||||||||
|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|
| 1 | 2 | 3 | 4 | 5 | 6 | 7 | 8 | 9 | 10 | 11 | 12 | 13 | 14 | 15 | 16 | 17 | 18 | |||||||||||||||
| 1 | H | He | ||||||||||||||||||||||||||||||
| 2 | Li | Be | B | C | N | O | F | Ne | ||||||||||||||||||||||||
| 3 | Na | Mg | Al | Si | P | S | Cl | Ar | ||||||||||||||||||||||||
| 4 | K | Ca | Sc | Ti | V | Cr | Mn | Fe | Co | Ni | Cu | Zn | Ga | Ge | As | Se | Br | Kr | ||||||||||||||
| 5 | Rb | Sr | Y | Zr | Nb | Mo | Tc | Ru | Rh | Pd | Ag | Cd | In | Sn | Sb | Te | I | Xe | ||||||||||||||
| 6 | Cs | Ba | La | Ce | Pr | Nd | Pm | Sm | Eu | Gd | Tb | Dy | Ho | Er | Tm | Yb | Lu | Hf | Ta | W | Re | Os | Ir | Pt | Au | Hg | Tl | Pb | Bi | Po | At | Rn |
| 7 | Fr | Ra | Ac | Th | Pa | U | Np | Pu | Am | Cm | Bk | Cf | Es | Fm | Md | No | Lr | Rf | Db | Sg | Bh | Hs | Mt | Ds | Rg | Cn | Uut | Fl | Uup | Lv | Uus | Uuo |
| 8 | Uue | Ubn | Ubu | Ubb | Ubt | Ubq | Ubp | Ubh | ||||||||||||||||||||||||
щёлочноземельные металлы в, щёлочноземельные металлы и, щёлочноземельные металлы химия, щёлочноземельные металлын
Часть первая. Общая характеристика II А группы Периодической Системы элементов.
В этой группе располагаются следующие элементы: Be, Mg, Ca, Sr, Ba, Ra. Они имеют общую электронную конфигурацию: (n-1)p 6 ns 2 , кроме Ве 1s 2 2s 2 . В силу последнего, свойства Ве немного отличаются от свойств подгруппы в целом. Свойства магния тоже отличаются от свойств подгруппы, но в меньшей степени. В ряду Са – Sr – Ba – Ra свойства меняются последовательно. Относительная электроотрицательность в ряду Ве – Ra падает т.к. с увеличением размера атома валентные электроны отдаются охотнее. Свойства элементов IIА подгруппы определяются легкостью отдачи двух ns-электронов. При этом образуются ионы Э 2+ . При изучении дифракции рентгеновских лучей выяснилось, что в некоторых соединениях элементы IIА подгруппы проявляют одновалентность. Примером таких соединения являются ЭГ, которые получаются при добавлении Э к расплаву ЭГ 2 . Все элементы этого ряда не встречаются в природе в свободном состоянии ввиду высокой активности.
Часть вторая. Бериллий и магний.
История бериллия
Соединения бериллия в виде драгоценных камней были известны еще в древности. С давних пор люди искали и разрабатывали месторождения голубых аквамаринов, зеленых изумрудов, зеленовато-желтых бериллов и золотистых хризобериллов. Но только в конце 18 века химики заподозрили, что в бериллах есть какой-то новый неизвестный элемент. В 1798 году французский химик Льюис Николас Воклен выделил из берилла окись "La terree du beril", отличавшуюся от окиси алюминия. Эта окись придавала солям сладкий вкус, не образовывала квасцов, растворялась в растворе карбоната аммония и не осаждалась оксалатом калия. Металлический бериллий был впервые получен в 1829 году известным немецким ученым Веллером и одновременно французским ученым Бюсси, который получил порошок металлического бериллия восстановлением хлористого бериллия металлическим калием. Начало промышленного производства относится к 30-40 гг. прошлого столетия.
История магния
Свое название элемент получил по местности Магнезия в Древней Греции.Природные магнийсодержащие материалы магнезит и доломит издавна использовались в строительстве.
Первые попытки выделить металлическую основу магнезии в чистом виде были предприняты в начале XIX в. знаменитым английским физиком и химиком Гемфри Дэви (1778–1829) после того, как он подверг электролизу расплавы едкого кали и едкого натра и получил металлический Na и K. Он решил попытаться аналогичным образом осуществить разложение оксидов щелочноземельных металлов и магнезии. В своих первоначальных опытах Дэви пропускал ток через влажные оксиды, предохраняя их от соприкосновения с воздухом слоем нефти; однако при этом металлы сплавлялись с катодом и их не удавалось отделить.
Дэви пробовал применять множество различных методов, но все они по разным причинам оказывались малоуспешными. Наконец, в 1808 г. его постигла удача – он смешал влажную магнезию с оксидом ртути, поместил массу на пластинку из платины и пропустил через нее ток; амальгаму перенес в стеклянную трубку, нагрел, чтобы удалить ртуть, и получил новый металл. Тем же способом Дэви удалось получить барий, кальций и стронций. Промышленное производство магния электролитическим способом было начато в Германии в конце 19 века. Теоретические и экспериментальные работы по получению магния электролитическим способом в нашей стране были выполнены П.П. Федотьевым; процесс восстановления оксида магния кремнием в вакууме исследовал П.Ф. Антипин.
Распространение
Бериллий относится к числу не очень распространенных элементов: его содержание в земной коре составляет 0,0004 вес. %. Бериллий в природе находится в связанном состоянии. Важнейшие минералы бериллия: берилл- Be 3 Al 2 (SiO 3) 6 , хризоберилл- Be(AlO 2) 2 и фенакит- Be 2 SiO 4 . Основная часть бериллия распылена в качестве примесей к минералам ряда других элементов, особенно алюминия. Бериллий содержится также в глубинных осадках морей и золе некоторых каменных углей. Некоторые разновидности берилла, окрашенные примесями в различные цвета, относятся к драгоценным камням. Таковы, например, зеленые изумруды, голубовато-зеленые аквамарины.
Магний – один из самых распространенных в земной коре элементов. Содержание магния составляет 1,4 %. К числу важнейших минералов относятся, в частности, углекислые карбонатные породы, образующие огромные массивы на суше и даже целые горные хребты – магнезит MgCO 3 и доломит MgCO 3 -CaCO 3 . Под слоями различных наносных пород совместно с залежами каменной соли известны колоссальные залежи и другого легкорастворимого магнийсодержащего минерала – карналлита MgCl 2 -KCl-6H 2 O. Кроме того, во многих минералах магний тесно связан с кремнеземом, образуя, например, оливин [(Mg, Fe) 2 SiO 4 ] и реже встречающийся форстерит (Mg 2 SiO 4). Другие магнийсодержащие минералы – это бруцит Mg(OH) 2 , кизерит MgSO 4 , эпсонит MgSO 4 -7H 2 O, каинит MgSO 4 -KCl-3H 2 O. На поверхности Земли магний легко образует водные силикаты (тальк, асбест и др.), примером которых может служить серпентин 3MgO-2SiO 2 -2H 2 O. Из известных минералов около 13 % содержат магний. Однако природные соединения магния широко встречаются и в растворенном виде. Кроме различных минералов и горных пород, 0,13 % магния в виде MgCl 2 постоянно содержатся в водах океана (его запасы здесь неисчерпаемы – около 6-10 16 т) и в соленых озерах и источниках. Магний также входит в состав хлорофилла в количестве до 2 % и выступает здесь как комплексообразователь. Общее содержание этого элемента в живом веществе Земли оценивается величиной порядка 10 11 тонн.
Получение
Основной (около 70%) способ получения магния – электролиз расплавленного карналлита или MgCl 2 под слоем флюса для защиты от окисления. Термический способ получения магния (около 30%) заключается в восстановлении обожженного магнезита или доломита. Бериллиевые концентраты перерабатывают в оксид или гидроксид бериллия, из которых получают фторид или хлорид. При получении металлического бериллия осуществляют электролиз расплава BeCl 2 (50 вес.%) и NaCl.Такая смесь имеет температуру плавления 300 о С против 400 о С для чистого ВеCl 2 . Также бериллий получают магний- или алюмотермически при 1000-1200 0 C из Na 2 : Na 2 + 2Mg = Be + 2Na + МgF 2 . Особо чистый бериллий (в основном для атомной промышленности) получают зонной плавкой, дистилляцией в вакууме и электролитическим рафинированием.
Особенности
Бериллий является “чистым” элементом. В природе магний встречается в виде трех стабильных изотопов: 24 Mg (78,60%), 25 Mg (10,11%) и 26 Mg (11,29%). Искусственно были получены изотопы с массами 23, 27 и 28.
Бериллий имеет атомный номер 4 и атомный вес 9,0122. Он находится во втором периоде периодической системы и возглавляет главную подгруппу 2 группы. Электронная структура атома бериллия - 1s 2 2s 2 . При химическом взаимодействии атом бериллия возбуждается (что требует затраты 63 ккал/г×атом) и один из 2s-электронов переходит на 2р-орбиталь что определяет специфику химии бериллия: он может проявлять максимальную ковалентность, равную 4, образуя 2 связи по обменному механизму, и 2 по донорно-акцепторному. На кривой потенциалов ионизации бериллий занимает одно из верхних мест. Последнее соответствует его малому радиусу и характеризует бериллий как элемент не особенно охотно отдающий свои электроны, что в первую очередь определяет малую степень химической активности элемента. С точки зрения электроотрицательности бериллий может рассматриваться как типичный переходный элемент между электроположительными атомами металлов, легко отдающих свои электроны, и типичными комплексо-образователями, имеющими тенденцию к образованию ковалентной связи. Бериллий проявляет диагональную аналогию с алюминием в большей мере, чем LicMg и является кайносимметричным элементом. Бериллий и его соединения весьма токсичны. ПДК в воздухе - 2 мкг/м 3 .
В периодической системе элементов магний располагается в главной подгруппе II группы; порядковый номер магния – 12, атомный вес 24,312. Электронная конфигурация невозбужденного атома – 1s 2 2s 2 2p 6 3s 2 ; строение внешних электронных оболочек атома Mg (3s 2) соответствует его нульвалентному состоянию. Возбуждение до двухвалентного 3s 1 3p 1 требует затраты 62 ккал/г-атом. Ионизационные потенциалы магния меньше, чем бериллия, поэтому соединения магния характеризуются большей долей ионности связи. По комплексообразовательной способности магний тоже уступает бериллию. Взаимодействие с элементами IIIВ группы с недостроенными d-оболочками имеет некоторые особенности. В эту группу входят Sc, Y, Ln, и Th. Эти элементы образуют с магнием ряд промежуточных фаз и хорошо растворяются в нем в жидком состоянии. Диаграммы состояния смесей этих элементов с магнием – эвтектического характера. Растворимость этих элементов в магнии в твердом состоянии не велика (2 – 5 % по массе). Со щелочноземельными и особенно со щелочными металлами магний не образует значительной области растворимости в твердом состоянии, что связано с большим различием атомных радиусов. Исключением является литий, атомный радиус которого отличается от атомного радиуса магния на 2 %. Системы магния с медью, серебром и золотом – эвтектического типа. Растворимость серебра при температуре эвтектики –16 % по массе.
Физические свойства
Бериллий – металл серебристо-белого цвета. Довольно тверд и хрупок. Обладает диамагнитными свойствами. На воздухе он покрывается тонкой окисной пленкой предающей металлу серый, матовый цвет и предохраняющей от дальнейшей коррозии. Сжимаемость бериллия очень мала. Меньше всех металлов (в 17 раз меньше Аl) задерживает рентгеновское излучение. Он кристаллизуется в ГПУ-структуре с периодами а=0,228 нм, и с=0,358 нм, КЧ=6. При 1254 о С гексагональная a-модификация переходит в кубическую b. Бериллий образует эвтектические сплавы с Al и Si.
НАХОЖДЕНИЕ В ПРИРОДЕ
В земной коре содержится бериллия - 0,00053%, магния - 1,95%, кальция - 3,38%, стронция - 0,014%, бария - 0,026%, радий - искусственный элемент.
Встречаются в природе только в виде соединений - силикатов, алюмосиликатов, карбонатов, фосфатов, сульфатов и т.д.
ПОЛУЧЕНИЕ
1. Бериллий получают восстановлением фторида:
BeF 2 + Mg t ˚ C → Be + MgF 2
2. Барий получают восстановлением оксида:
3BaO + 2Al t ˚ C → 3Ba + Al 2 O 3
3. Остальные металлы получают электролизом расплавов хлоридов:
Т.к. металлы данной подгруппы сильные восстановители, то получение возможно только путем электролиза расплавов солей. В случае Са обычно используют CaCl 2 (c добавкой CaF 2 для снижения температуры плавления)
CaCl 2 =Ca+Cl 2
ФИЗИЧЕСКИЕ СВОЙСТВА
Щелочноземельные металлы (по сравнению со щелочными металлами) обладают более высокими t°пл. и t°кип, плотностями и твердостью.
ПРИМЕНЕНИЕ
| Бериллий (Амфотерен) | Магний | Ca, Sr, Ba, Ra |
| 1. Изготовление теплозащитных конструкций для косм. кораблей (жаропрочность, теплоёмкость бериллия) 2. Бериллиевые бронзы (лёгкость, твёрдость, жаростойкость, антикоррозионность сплавов, прочность на разрыв выше стали, можно прокатывать в ленты толщиной 0,1 мм) 3. В атомных реакторах, рентгенотехнике, радиоэлектронике 4. Сплав Be, Ni, W- в Швейцарии делают пружины для часов Но Be –хрупок, ядовит и очень дорогой | 1. Получение металлов – магнийтермия (титан, уран, цирконий и др) 2. Для получения сверхлёгких сплавов (самолётостроение, производство автомобилей) 3. В оргсинтезе 4. Для изготовления осветительных и зажигательных ракет. | 1. Изготовление свинцово-кадмиевых сплавов, необходимых при производстве подшипников. 2. Стронций – восстановитель в производстве урана. Люминофоры - соли стронция. 3. Используют в качестве геттеров, веществ для создания вакуума в электроприборах. Кальций Получение редких металлов, входит в состав сплавов. Барий Газопоглотитель в электронно-лучевых трубках. Радий Рентгенодиагностика, исследовательские работы. |
ХИМИЧЕСКИЕ СВОЙСТВА
1. Очень реакционноспособны, сильные восстановители. Активность металлов и их восстановительная способность увеличивается в ряду: Be–Mg–Ca–Sr–Ba
2. Обладают степенью окисления +2.
3. Реагируют с водой при комнатной температуре (кроме Be) с выделением водорода.
4. С водородом образуют солеобразные гидриды ЭH 2 .
5. Оксиды имеют общую формулу ЭО. Тенденция к образованию пероксидов выражена слабее, чем для щелочных металлов.
Реакция с водой.
В обычных условиях поверхность Be и Mg покрыты инертной оксидной пленкой, поэтому они устойчивы по отношению к воде, но с горячей водой магний образует основание Mg(OH) 2.
В отличие от них Ca, Sr и Ba растворяются в воде с образованием гидроксидов, которые являются сильными основаниями:
Ве + H 2 O → ВеO+ H 2
Ca + 2H 2 O → Ca(OH) 2 + H 2
Реакция с кислородом.
Все металлы образуют оксиды RO, барий образует пероксид – BaO 2:
2Mg + O 2 → 2MgO
Ba + O 2 → BaO 2
3. С другими неметаллами образуются бинарные соединения:
Be + Cl 2 → BeCl 2 (галогениды)
Ba + S → BaS (сульфиды)
3Mg + N 2 → Mg 3 N 2 (нитриды)
Ca + H 2 → CaH 2 (гидриды)
Ca + 2C → CaC 2 (карбиды)
3Ba + 2P → Ba 3 P 2 (фосфиды)
Бериллий и магний сравнительно медленно реагируют с неметаллами.
4. Все металлы растворяются в кислотах:
Ca + 2HCl → CaCl 2 + H 2
Mg + H 2 SO 4 (разб.) → MgSO 4 + H 2
Бериллий также растворяется в водных растворах щелочей:
Be + 2NaOH + 2H 2 O → Na 2 + H 2
5. Качественная реакция на катионы щелочноземельных металлов – окрашивание пламени в следующие цвета:
Ca 2+ - темно-оранжевый
Sr 2+ - темно-красный
Ba 2+ - светло-зеленый
Катион Ba 2+ обычно открывают обменной реакцией с серной кислотой или ее солями:
BaCl 2 + H 2 SO 4 → BaSO 4 ↓ + 2HCl
Ba 2+ + SO 4 2- → BaSO 4 ↓
Сульфат бария – белый осадок, нерастворимый в минеральных кислотах.
Оксиды щелочноземельных металлов
Получение
1) Окисление металлов (кроме Ba, который образует пероксид)
2) Термическое разложение нитратов или карбонатов
CaCO 3 t ˚ C → CaO + CO 2
2Mg(NO 3) 2 t˚C → 2MgO + 4NO 2 + O 2
Химические свойства
Типичные основные оксиды. Реагируют с водой (кроме BeO и MgO), кислотными оксидами и кислотами
СаO + H 2 O → Са(OH) 2
3CaO + P 2 O 5 → Ca 3 (PO 4) 2
BeO + 2HNO 3 → Be(NO 3) 2 + H 2 O
BeO - амфотерный оксид, растворяется в щелочах:
BeO + 2NaOH + H 2 O → Na 2
Гидроксиды щелочноземельных металлов R(OH) 2
Получение
Реакции щелочноземельных металлов или их оксидов с водой:
Ba + 2H 2 O → Ba(OH) 2 + H 2
CaO (негашеная известь) + H 2 O → Ca(OH) 2 (гашеная известь)
Химические свойства
Гидроксиды R(OH) 2 - белые кристаллические вещества, в воде растворимы хуже, чем гидроксиды щелочных металлов (растворимость гидроксидов уменьшается с уменьшением порядкового номера; Be(OH) 2 – нерастворим в воде, растворяется в щелочах ). Основность R(OH) 2 увеличивается с увеличением атомного номера:
Be(OH) 2 – амфотерный гидроксид
Mg(OH) 2 – слабое основание
Са(OH) 2 - щелочь
остальные гидроксиды - сильные основания (щелочи).
1) Реакции с кислотными оксидами:
Ca(OH) 2 + СO 2 → CaСO 3 ↓ + H 2 O ! Качественная реакция на углекислый газ
Ba(OH) 2 + SO 2 → BaSO 3 ↓ + H 2 O
2) Реакции с кислотами:
Ba(OH) 2 + 2HNO 3 → Ba(NO 3) 2 + 2H 2 O
3) Реакции обмена с солями:
Ba(OH) 2 + K 2 SO 4 → BaSO 4 ↓+ 2KOH
4) Реакция гидроксида бериллия со щелочами:
Be(OH) 2 + 2NaOH → Na 2
Жесткость воды
Природная вода, содержащая ионы Ca 2+ и Mg 2+ , называется жесткой. Жесткая вода при кипячении образует накипь, в ней не развариваются пищевые продукты; моющие средства не дают пены.
Карбонатная (временная) жесткость обусловлена присутствием в воде гидрокарбонатов кальция и магния, некарбонатная (постоянная) жесткость – хлоридов и сульфатов.
Общая жесткость воды рассматривается как сумма карбонатной и некарбонатной.
Удаление жесткости воды осуществляется путем осаждения из раствора ионов Ca 2+ и Mg 2+
К щелочноземельным металлам относятся металлы IIa группы: бериллий, магний, кальций, стронций, барий и радий. Отличаются легкостью, мягкостью и сильной реакционной способностью.
Общая характеристика
От Be к Ra (сверху вниз в периодической таблице) происходит увеличение: атомного радиуса, металлических, основных, восстановительных свойств, реакционная способность. Уменьшается электроотрицательность, энергия ионизация, сродство к электрону.
Электронные конфигурации у данных элементов схожи, так как они находятся в одной группе (главной подгруппе!), общая формула ns 2:
- Be - 2s 2
- Mg - 3s 2
- Ca - 4s 2
- Sr - 5s 2
- Ba - 6s 2
- Ra - 7s 2
Природные соединения
В природе щелочноземельные металлы встречаются в виде следующих соединений:
- Be - BeO*Al 2 O 3 *6SiO 2 - берилл
- Mg - MgCO 3 - магнезит, MgO*Al 2 O 3 - шпинель, 2MgO*SiO 2 - оливин
- Ca - CaCO 3 - мел, мрамор, известняк, кальцит, CaSO 4 *2H 2 O - гипс, CaF 2 - флюорит

Получение
Это активные металлы, которые нельзя получить электролизом раствора. С целью их получения применяют электролиз расплавов, алюминотермию и вытеснением их из солей другими более активными металлами.
MgCl 2 → (t) Mg + Cl 2 (электролиз расплава)
CaO + Al → Al 2 O 3 + Ca (алюминотермия - способ получения металлов путем восстановления их оксидов алюминием)
MgBr 2 + Ca → CaBr 2 + Mg

Химические свойства

Оксиды щелочноземельных металлов
Имеют общую формулу RO, например: MgO, CaO, BaO.
Получение
Оксиды щелочноземельных металлов можно получить путем разложения карбонатов и нитратов:
MgCO 3 → (t) MgO + CO 2
Ca(NO 3) 2 → (t) CaO + O 2 + NO 2
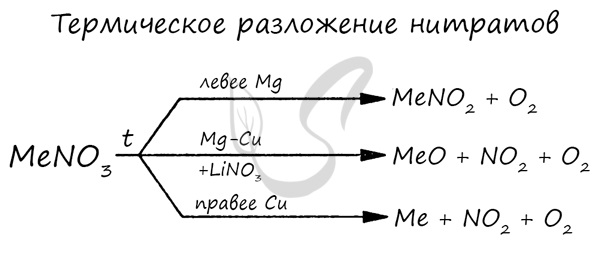
Химические свойства
Проявляют преимущественно основные свойства, все кроме BeO - амфотерного оксида.

Гидроксиды щелочноземельных металлов
Проявляют основные свойства, за исключением гидроксида бериллия - амфотерного гидроксида.
Получение
Получают гидроксиды в реакции соответствующего оксида металла и воды (все кроме Be(OH) 2)
CaO + H 2 O → Ca(OH) 2
Химические свойства
Основные свойства большинства гидроксидов располагают к реакциям с кислотами и кислотными оксидами.
Ba(OH) 2 + H 2 SO 4 → BaSO 4 ↓ + H 2 O
Ca(OH) 2 + H 2 O + CO 2 → Ca(HCO 3) 2 + H 2 O
Ca(HCO 3) 2 + Ca(OH) 2 → CaCO 3 + H 2 O + CO 2
Ca(OH) 2 + CO 2 → CaCO 3 ↓ + H 2 O

Реакция с солями (и не только) идут в том случае, если соль растворимы и по итогам реакции выделяется газ, выпадает осадок или образуется слабый электролит (вода).
Ba(OH) 2 + Na 2 SO 4 → BaSO 4 ↓ + NaOH
Гидроксид бериллия относится к амфотерным: проявляет двойственные свойства, реагируя и с кислотами, и с основаниями.
Be(OH) 2 + HCl → BeCl 2 + H 2 O
Be(OH) 2 + NaOH → Na 2
Жесткостью воды называют совокупность свойств воды, зависящая от присутствия в ней преимущественно солей кальция и магния: гидрокарбонатов, сульфатов и хлоридов.
Различают временную (карбонатную) и постоянную (некарбонатную) жесткость.

Вероятно, вы часто устраняете жесткость воды у себя дома, осмелюсь предположить - каждый день. Временная жесткость воды устраняется обычным кипячением воды в чайнике, и известь на его стенках - CaCO 3 - бесспорное доказательство устранения жесткости:
Ca(HCO 3) 2 → CaCO 3 ↓ + CO 2 + H 2 O
Также временную жесткость можно устранить, добавив Na 2 CO 3 в воду:
Ca(HCO 3) 2 + Na 2 CO 3 → CaCO 3 ↓ + NaHCO 3
С постоянной жесткостью бороться кипячением бесполезно: сульфаты и хлориды не выпадут в осадок при кипячении. Постоянную жесткость воды устраняют добавлением в воду Na 2 CO 3:
CaCl 2 + Na 2 CO 3 → CaCO 3 ↓ + NaCl
MgSO 4 + Na 2 CO 3 + H 2 O → 2 CO 3 ↓ + CO 2 + Na 2 SO 4
Жесткость воды можно определить с помощью различных тестов. Чрезмерно высокая жесткость воды приводит к быстрому образованию накипи на стенках котлов, труб, чайника.

©Беллевич Юрий Сергеевич
Данная статья написана Беллевичем Юрием Сергеевичем и является его интеллектуальной собственностью. Копирование, распространение (в том числе путем копирования на другие сайты и ресурсы в Интернете) или любое иное использование информации и объектов без предварительного согласия правообладателя преследуется по закону. Для получения материалов статьи и разрешения их использования, обратитесь, пожалуйста, к
- Классный час "Сдадим ОГЭ успешно" (9 класс)
- Как разгадывать ребусы с буквами и картинками: правила, советы, рекомендации
- Тема любви в творчестве, лирике есенина сочинение Мое восприятие темы любви в лирике есенина
- Декартовы координаты точек плоскости
- Картотека игровых упражнений для обучения детей с нарушением речи правильному употреблению предлогов Д игра где что находится предлоги
- Как определяют происхождение метеоритных кратеров
- Какие открытия сделал физик Эрнест Резерфорд?

 Live Journal
Live Journal Facebook
Facebook Twitter
Twitter